泰國是公共醫(yī)療非常有特色的國家之一�,政府為泰國民眾體用了非常廉價的公共醫(yī)療,泰國也有非常良好的醫(yī)療器械產業(yè)及醫(yī)療器械市場�,本文為大家介紹泰國醫(yī)療器械注冊基礎知識。
泰國是公共醫(yī)療非常有特色的國家之一�,政府為泰國民眾體用了非常廉價的公共醫(yī)療,泰國也有非常良好的醫(yī)療器械產業(yè)及醫(yī)療器械市場�,本文為大家介紹泰國醫(yī)療器械注冊基礎知識。
一�、泰國醫(yī)療器械注冊監(jiān)管機構(TFDA)簡介
TFDA是泰國食品藥品監(jiān)督管理局(Thailand Food and Drug Administration) ,進入泰國的化妝品�、醫(yī)療器械,食品,藥品�,補充劑,用于保健的產品或其他醫(yī)學�,麻醉和有毒物質均需要泰國食品藥品監(jiān)督管理局(FDA)注冊。
由于泰國的國內醫(yī)療設備制造商通常只生產基本醫(yī)療產品�,例如注射器和手套。因此, 該國 依賴國外進口復雜或高端的醫(yī)療設備,這為西方醫(yī)療器械制造商提供了重要的進口機會�。 醫(yī)療器械由泰國食品藥品監(jiān)督管理局(FDA)的醫(yī)療器械控制部(MDCO)監(jiān)管,其任務是監(jiān)管和監(jiān)視健康產品�,以滿足質量和功效要求。醫(yī)療器械受《醫(yī)療設備法案B.E.2531年(1988)》監(jiān)管�。
此外,辦理泰國醫(yī)療器械注冊的企業(yè)還需要認識泰國醫(yī)療器械監(jiān)管機構�,如下:
1.泰國食品藥品監(jiān)督管理局(TFDA) 是負責監(jiān)管泰國醫(yī)療器械的政府機構。
2.醫(yī)療器械控制部是TFDA的辦公室,專門負責醫(yī)療器械事務的監(jiān)督�。
二、泰國對醫(yī)療器械有哪些不同的監(jiān)管分類�?
為了使泰國的醫(yī)療器械法規(guī)與東盟醫(yī)療器械指令(AMDD)保持一致,泰國公共衛(wèi)生部發(fā)布自2019年12月19日起�,醫(yī)療器械分為:
(1)體外診斷醫(yī)療設備;
(2)非體外診斷醫(yī)療器械。
體外診斷醫(yī)療器械按對個人和公共健康的危害程度從低到高分類:
風險等級 | 醫(yī)療器械分類等級 |
低個人和公共健康風險 | 1級 |
中個人�、低公共健康風險 | 2級 |
高個人、中公共健康風險 | 3級 |
高個人�、中公共健康風險 | 4級 |
其它醫(yī)療器械分類類似,如下圖所示:
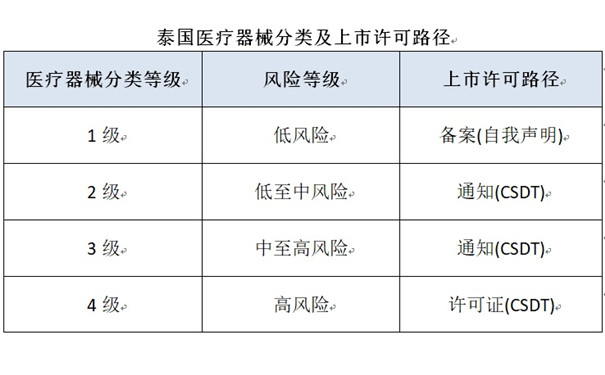
醫(yī)療器械注冊要求因設備類別而異�。低風險的 I 類設備必須在泰國進口和銷售之前列名�,而 II 類和 III 類設備必須得到通知�,IV 類設備必須獲得批準的許可證才能投放泰國市場。II�、III 和 IV 類器械需要按照東盟 CSDT 格式提交技術檔案。I 類無菌和測量設備需要提交測試報告才能將這些設備投放市場�。
三、泰國醫(yī)療器械注冊流程
泰國醫(yī)療器械注冊流程根據對應的產品級別選擇相應的流程�,TFDA注冊是很和流程如下:醫(yī)療器械判定-選擇審核路徑-自由銷售證書-CSDT檔案-申請人有醫(yī)療器械經營資質-產品清單-注冊通過。泰國醫(yī)療器械注冊申請條件有哪些�?1.申請者須有完善的產品貯存計劃,包括指示放置醫(yī)療器械的存放地點內部平面圖�,并詳細說明倉儲空間的空間分配、存儲設施安裝�、和減低存貨對個人和公共健康的方案。
2.療器械在進入泰國之前需要有生產過的醫(yī)療器械注冊證明�。非泰國本地生產的醫(yī)療器械產品很難單靠在其他國家的醫(yī)療器械注冊認證進行泰國FDA認證。如果有合理的原因�,可以為無原產國醫(yī)療器械注冊證的產品申請?zhí)﹪t(yī)療器械注冊,如:產品是專為原產國以外的人群使用�。
四、泰國代理人要求
對于在泰國當地沒有子公司的客戶�、沒有可以持證資質的泰國總經銷商,或者不希望將產品的認證綁定在一批經銷商身上�,找一個獨立的泰國公司是一個好的選擇。更多泰國醫(yī)療器械注冊代辦服務需求�,歡迎您隨時方便與杭州證標客醫(yī)藥技術咨詢有限公司聯(lián)絡�,聯(lián)系人:葉工�,電話:18058734169�,微信同。