醫(yī)用呼吸道濕化器一般由主機(jī)�、貯水箱和一些附件組成,是用于濕化輸送給患者的呼吸氣體的醫(yī)用電氣設(shè)備�����,通常與呼吸治療設(shè)備配合使用�����。按照我國(guó)醫(yī)療器械分類(lèi)規(guī)則�,醫(yī)用呼吸道濕化器產(chǎn)品屬于第二類(lèi)醫(yī)療器械注冊(cè)產(chǎn)品,分類(lèi)編碼為08-05-02�。
引言:醫(yī)用呼吸道濕化器一般由主機(jī)、貯水箱和一些附件組成�����,是用于濕化輸送給患者的呼吸氣體的醫(yī)用電氣設(shè)備�����,通常與呼吸治療設(shè)備配合使用�。按照我國(guó)醫(yī)療器械分類(lèi)規(guī)則,醫(yī)用呼吸道濕化器產(chǎn)品屬于第二類(lèi)醫(yī)療器械注冊(cè)產(chǎn)品�,分類(lèi)編碼為08-05-02。
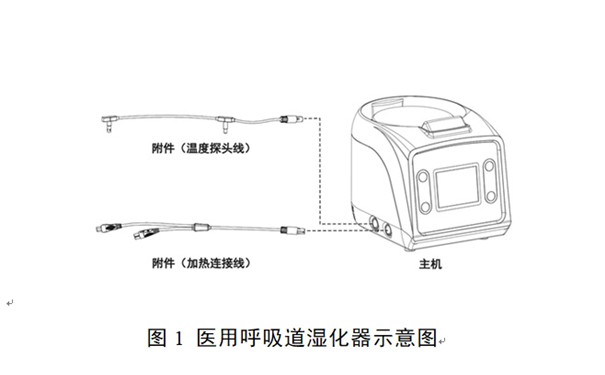
一�、醫(yī)用呼吸道濕化器注冊(cè)流程:
醫(yī)用呼吸道濕化器注冊(cè)單元?jiǎng)澐郑?/span>注冊(cè)單元按照《醫(yī)療器械注冊(cè)單元?jiǎng)澐种笇?dǎo)原則》的要求,原則上以產(chǎn)品的技術(shù)原理�、結(jié)構(gòu)組成、性能指標(biāo)和適用范圍為劃分依據(jù)�����。
加熱濕化控制技術(shù)原理差別較大的產(chǎn)品�����,建議劃分為不同的注冊(cè)單元�����。貯水箱�、氣體溫度傳感器、加熱連接線等部件可以和主機(jī)劃分為同一個(gè)注冊(cè)單元�。
醫(yī)用呼吸道濕化器注冊(cè)產(chǎn)品按照國(guó)產(chǎn)第二類(lèi)醫(yī)療器械申報(bào)流程,注冊(cè)流程如下:
前期準(zhǔn)備(廠房裝修�����、工藝布局、設(shè)備配置�、產(chǎn)品研發(fā)定型、實(shí)驗(yàn)室建設(shè))——建立醫(yī)療器械質(zhì)量管理體系——注冊(cè)檢測(cè)——臨床評(píng)價(jià)——注冊(cè)申請(qǐng)——技術(shù)審評(píng)(省藥監(jiān)局)——醫(yī)療器械注冊(cè)質(zhì)量管理體系核查——審評(píng)發(fā)補(bǔ)補(bǔ)正&體考不符合整改——行政許可——取得醫(yī)療器械產(chǎn)品注冊(cè)證——申請(qǐng)醫(yī)療器械生產(chǎn)許可證——取得醫(yī)療器械生產(chǎn)許可證�����。
二�、第二類(lèi)醫(yī)療器械注冊(cè)費(fèi)用:
醫(yī)用呼吸道濕化器作為第二類(lèi)醫(yī)療器械注冊(cè)產(chǎn)品,注冊(cè)費(fèi)用主要包括企業(yè)自身為具備醫(yī)療器械生產(chǎn)和產(chǎn)品研發(fā)�����、制造產(chǎn)生的費(fèi)用�;醫(yī)療器械注冊(cè)檢驗(yàn)及臨床評(píng)價(jià)需要的費(fèi)用;醫(yī)療器械注冊(cè)審評(píng)費(fèi)用�����;及第三方醫(yī)療器械咨詢(xún)服務(wù)公司收取的咨詢(xún)輔導(dǎo)費(fèi)用�����。
三�、醫(yī)用呼吸道濕化器注冊(cè)審評(píng)要點(diǎn):
1..適用范圍�����、禁忌證
1.1適用范圍
產(chǎn)品用于濕化輸送給患者的呼吸氣體。
適用人群:視產(chǎn)品設(shè)計(jì)�����,可以用于成人�、兒童、嬰兒等�。
適用環(huán)境:明確產(chǎn)品的使用場(chǎng)所,如醫(yī)院�����、家庭等使用場(chǎng)所�。
如果產(chǎn)品可以在特殊環(huán)境使用,也應(yīng)進(jìn)一步說(shuō)明�,如急救轉(zhuǎn)運(yùn)、高海拔條件下使用等�����。
1.2禁忌證:暫未發(fā)現(xiàn)�����。
2.產(chǎn)品技術(shù)要求應(yīng)包括的主要性能指標(biāo)
不同的醫(yī)用呼吸道濕化器產(chǎn)品其參數(shù)根據(jù)設(shè)計(jì)要求會(huì)有所區(qū)別。本指導(dǎo)原則列出此類(lèi)產(chǎn)品可能涉及的重要性能參數(shù)�����,注冊(cè)申請(qǐng)人可根據(jù)自身產(chǎn)品的技術(shù)特點(diǎn)制定性能指標(biāo)的具體要求�。若企業(yè)宣稱(chēng)產(chǎn)品還具有其他工作模式應(yīng)同時(shí)考慮制定相應(yīng)的性能和功能要求。
2.1主機(jī)技術(shù)指標(biāo)要求
以下指標(biāo)依據(jù)YY 9706.274標(biāo)準(zhǔn)要求列出�,若標(biāo)準(zhǔn)更新,申請(qǐng)人應(yīng)引用當(dāng)下現(xiàn)行標(biāo)準(zhǔn)�。申請(qǐng)人要求若高于標(biāo)準(zhǔn)可按申請(qǐng)人要求執(zhí)行。
2.1.1氣體流量范圍及濕化輸出:應(yīng)明確不同條件下的氣體流量范圍及對(duì)應(yīng)的氣體濕化輸出�����;
2.1.2被測(cè)氣體溫度監(jiān)護(hù)裝置:溫度顯示范圍:至少為25-45℃�,精度:≤±2℃;
2.1.3運(yùn)行噪音(距設(shè)備1米):≤50dB(A)�����;
2.1.4操作者可設(shè)置參數(shù):應(yīng)明確操作者可設(shè)置的參數(shù)�����,預(yù)期用于有創(chuàng)通氣治療的至少應(yīng)包括患者端氣體溫度設(shè)置;
2.1.5參數(shù)鎖定功能(如適用):包括輸送氣體溫度鎖定�;
2.1.6預(yù)熱時(shí)間:應(yīng)明確最大預(yù)熱時(shí)間;
2.1.7報(bào)警裝置(如適用):如患者端超溫報(bào)警�����、患者端低溫報(bào)警�����、患者端低濕度報(bào)警�、水量低報(bào)警或缺水報(bào)警�、主機(jī)加熱模塊超溫報(bào)警,應(yīng)符合YY 9706.108的規(guī)定�����。
2.2貯水箱性能指標(biāo)要求(如有)
2.2.1貯水容量
應(yīng)明確最大水位線的容量�����;
2.2.2接頭
圓錐接頭應(yīng)符合YY/T 1040.1接頭要求�;
2.2.3最大承受壓力
應(yīng)明確最大承受壓力,持續(xù)3min�����,應(yīng)無(wú)開(kāi)裂現(xiàn)象;
2.2.4液體密封性
加水至最大水位線時(shí)�,加入最大承受氣壓,應(yīng)無(wú)滲漏現(xiàn)象�����;
2.2.5無(wú)菌或微生物限度
若出廠是為無(wú)菌狀態(tài)�����,則應(yīng)制定無(wú)菌指標(biāo)�。使用前無(wú)需清潔、消毒的非無(wú)菌使用產(chǎn)品�,應(yīng)對(duì)其微生物限度進(jìn)行評(píng)價(jià),同時(shí)可參考《中華人民共和國(guó)藥典》中微生物限度藥典檢查法進(jìn)行檢測(cè)�;
環(huán)氧乙烷殘留量:若經(jīng)環(huán)氧乙烷滅菌,則環(huán)氧乙烷殘留量指標(biāo)應(yīng)符合GB/T 16886.7的要求�;
微生物限度限值要求:使用前無(wú)需清潔、消毒的非無(wú)菌使用產(chǎn)品�����,不得檢出大腸菌群、致病性化膿菌�����;細(xì)菌總數(shù)應(yīng)≤200cfu/g�、真菌菌落總數(shù)≤100cfu/g。
2.3軟件功能
應(yīng)符合《醫(yī)療器械軟件注冊(cè)審查指導(dǎo)原則》中第九章注冊(cè)申報(bào)資料補(bǔ)充說(shuō)明中關(guān)于產(chǎn)品技術(shù)要求性能指標(biāo)的建議內(nèi)容�。
2.4安全要求
產(chǎn)品應(yīng)符合GB 9706.1、YY 9706.274�����、YY 9706.102�����、YY 9706.108(如有)標(biāo)準(zhǔn)的要求�。
對(duì)于預(yù)期在家庭環(huán)境或其他非專(zhuān)業(yè)醫(yī)療環(huán)境下使用的設(shè)備�����,應(yīng)符合YY 9706.111標(biāo)準(zhǔn)的要求�。
3.同一注冊(cè)單元內(nèi)檢驗(yàn)典型性產(chǎn)品確定原則
3.1典型產(chǎn)品應(yīng)是同一注冊(cè)單元內(nèi)能夠代表本單元內(nèi)其他產(chǎn)品安全性和有效性的產(chǎn)品。
3.2產(chǎn)品的加熱濕化控制�、濕化罐結(jié)構(gòu)設(shè)計(jì)等因素決定了產(chǎn)品的性能,如果前述因素差別較大,應(yīng)分別進(jìn)行驗(yàn)證�。