關(guān)于醫(yī)療器械臨床評價���,等同于醫(yī)療器械臨床試驗(yàn)嗎����?結(jié)合近日藥監(jiān)總局發(fā)布的醫(yī)療器械分類子目錄醫(yī)療器械臨床評價推薦路徑���,一起聊聊醫(yī)療器械臨床評價的幾種方式����。
關(guān)于醫(yī)療器械臨床評價���,等同于醫(yī)療器械臨床試驗(yàn)嗎?結(jié)合近日藥監(jiān)總局發(fā)布的醫(yī)療器械分類子目錄醫(yī)療器械臨床評價推薦路徑���,一起聊聊醫(yī)療器械臨床評價的幾種方式����。
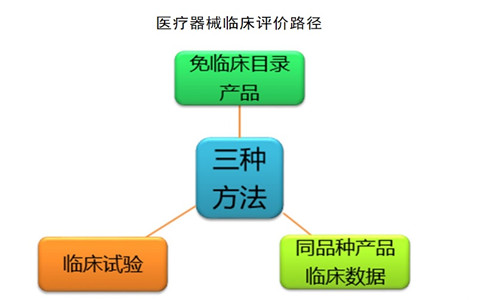
醫(yī)療器械臨床評價路徑有幾種���?
根據(jù)《醫(yī)療器械臨床評價技術(shù)指導(dǎo)原則(2021年第73號)》中內(nèi)容���,包括如上圖所示的三種途徑:
1.免于臨床試驗(yàn)?zāi)夸浿械尼t(yī)療器械臨床評價:
免于醫(yī)療器械臨床試驗(yàn)不等于免于醫(yī)療器械臨床評價����,企業(yè)仍然需要對照醫(yī)療器械分類目錄及醫(yī)療器械免臨床目錄���,完成醫(yī)療器械臨床評價內(nèi)容����。
2.通過同品種醫(yī)療器械臨床數(shù)據(jù)進(jìn)行分析����、評價:
(1)通過等同器械的臨床數(shù)據(jù)進(jìn)行臨床評價;
(2)使用可比器械的臨床數(shù)據(jù)進(jìn)行部分臨床評價���。
3.通過臨床試驗(yàn)數(shù)據(jù)進(jìn)行分析����、評價:
臨床試驗(yàn)包括在中國境內(nèi)開展的臨床試驗(yàn)����,在中國境外開展的臨床試驗(yàn)、多區(qū)域臨床試驗(yàn)����。
醫(yī)療器械注冊人可根據(jù)申報(bào)產(chǎn)品的技術(shù)特征����、適用范圍���、已有臨床數(shù)據(jù)等具體情況���,選擇恰當(dāng)?shù)脑u價途徑或者評價路徑的組合,開展臨床評價���。