眼科激光光凝機(jī)注冊(cè)審查指導(dǎo)原則(2022年第6號(hào))���,旨在指導(dǎo)注冊(cè)申請(qǐng)人對(duì)眼科激光光凝機(jī)注冊(cè)申報(bào)資料的準(zhǔn)備及撰寫,同時(shí)也為技術(shù)審評(píng)部門提供參考��。
眼科激光光凝機(jī)注冊(cè)審查指導(dǎo)原則
本指導(dǎo)原則旨在指導(dǎo)注冊(cè)申請(qǐng)人對(duì)眼科激光光凝機(jī)注冊(cè)申報(bào)資料的準(zhǔn)備及撰寫�,同時(shí)也為技術(shù)審評(píng)部門提供參考���。
本指導(dǎo)原則是對(duì)眼科激光光凝機(jī)的一般要求�,注冊(cè)申請(qǐng)人應(yīng)依據(jù)產(chǎn)品的具體特性確定其中內(nèi)容是否適用���。若不適用�,需具體闡述理由及相應(yīng)的科學(xué)依據(jù)���,并依據(jù)產(chǎn)品的具體特性對(duì)注冊(cè)申報(bào)資料的內(nèi)容進(jìn)行充實(shí)和細(xì)化��。
本指導(dǎo)原則是供注冊(cè)申請(qǐng)人和技術(shù)審評(píng)人員使用的指導(dǎo)性文件��,但不包括審評(píng)審批所涉及的行政事項(xiàng)���,亦不作為法規(guī)強(qiáng)制執(zhí)行�,應(yīng)在遵循相關(guān)法規(guī)的前提下使用本指導(dǎo)原則���。如果有能夠滿足相關(guān)法規(guī)要求的其他方法��,也可以采用���,但是需要提供詳細(xì)的研究資料和驗(yàn)證資料。
本指導(dǎo)原則是在現(xiàn)行法規(guī)和標(biāo)準(zhǔn)體系以及當(dāng)前認(rèn)知水平下制定���,隨著法規(guī)和標(biāo)準(zhǔn)的不斷完善�,以及科學(xué)技術(shù)的不斷發(fā)展�,相關(guān)內(nèi)容也將適時(shí)進(jìn)行調(diào)整。
一�、適用范圍
本指導(dǎo)原則適用于利用激光作用于生物組織產(chǎn)生熱效應(yīng),預(yù)期用于治療視網(wǎng)膜病變的眼科激光設(shè)備��。根據(jù)2017版《醫(yī)療器械分類目錄》��,產(chǎn)品管理類別為第三類��,分類編碼為16-05-02���。
二�、注冊(cè)審查要點(diǎn)
(一)監(jiān)管信息
1.產(chǎn)品名稱
應(yīng)為通用名稱,并符合《醫(yī)療器械通用名稱命名規(guī)則》和國(guó)家標(biāo)準(zhǔn)���、行業(yè)標(biāo)準(zhǔn)中的通用名稱要求�。產(chǎn)品名稱由一個(gè)核心詞和不超過(guò)三個(gè)的特征詞組成�。產(chǎn)品僅用于通過(guò)光熱效應(yīng)作用于眼組織,產(chǎn)生凝固的效果用于治療視網(wǎng)膜疾病的目的�,核心詞應(yīng)為激光光凝機(jī)。若產(chǎn)品的作用機(jī)理同時(shí)包含了光致爆破效應(yīng)�,可命名為激光治療機(jī)���。
通常情況下�,激光設(shè)備的三個(gè)特征詞應(yīng)包含脈沖特性�、工作物質(zhì)和技術(shù)特征詞,特征詞中多工作物質(zhì)可以缺省��。產(chǎn)品名稱中�,核心詞應(yīng)體現(xiàn)激光設(shè)備光凝/治療的特征。特征詞通常應(yīng)包含眼科��,如眼科半導(dǎo)體激光光凝機(jī)���;若申報(bào)產(chǎn)品的適用范圍不局限于眼科��,可不體現(xiàn)�,如倍頻固體激光治療機(jī)。特征詞還應(yīng)根據(jù)光凝機(jī)的工作物質(zhì)���,進(jìn)一步說(shuō)明產(chǎn)品特點(diǎn)�,如倍頻Nd:YAG���、半導(dǎo)體��、倍頻Nd:YVO4等��。若申報(bào)產(chǎn)品可激發(fā)產(chǎn)生不同波長(zhǎng)的激光���,特征詞可增加雙波長(zhǎng)或多波長(zhǎng)的描述,如眼科多波長(zhǎng)固體激光治療機(jī)��。
2.注冊(cè)單元?jiǎng)澐?/p>
根據(jù)《醫(yī)療器械注冊(cè)與備案管理辦法》第一百一十一條�,同時(shí)需參考《醫(yī)療器械注冊(cè)單元?jiǎng)澐种笇?dǎo)原則》的要求,原則上以產(chǎn)品的技術(shù)原理�、結(jié)構(gòu)組成、性能指標(biāo)和適用范圍為劃分依據(jù)�。結(jié)合光凝機(jī)產(chǎn)品技術(shù)點(diǎn)�,注冊(cè)單元?jiǎng)澐纸ㄗh符合以下原則:
(1)不同波長(zhǎng)的單一波長(zhǎng)激光設(shè)備應(yīng)劃分為不同的注冊(cè)單元�,例如激光器只產(chǎn)生532nm波長(zhǎng)與只產(chǎn)生577nm波長(zhǎng)的設(shè)備應(yīng)劃分為不同的注冊(cè)單元。同一設(shè)備若含多個(gè)波長(zhǎng)���,不涉及注冊(cè)單元?jiǎng)澐帧?/p>
(2)結(jié)構(gòu)組成不同的設(shè)備應(yīng)劃分為不同的注冊(cè)單元���,例如,激光主機(jī)需要和其他傳輸部件配合使用的設(shè)備�,與激光模塊和裂隙燈顯微鏡集成的設(shè)備,應(yīng)劃分為不同的注冊(cè)單元��。
3.結(jié)構(gòu)組成
應(yīng)概述光凝機(jī)關(guān)鍵部件并提供結(jié)構(gòu)示意圖�,一般包括主機(jī)、激光應(yīng)用部件(如眼內(nèi)光纖/裂隙燈顯微鏡/裂隙燈適配器/間接檢眼鏡)�、腳踏開關(guān)��、激光防護(hù)眼鏡等���。還應(yīng)詳述主機(jī)內(nèi)部的結(jié)構(gòu)��,明確光凝機(jī)�、光束傳輸部件��、光束掃描控制部件(如適用)的結(jié)構(gòu)。對(duì)于多種型號(hào)規(guī)格的產(chǎn)品��,應(yīng)列表和/或提供圖示���,說(shuō)明各型號(hào)之間的異同���,如:結(jié)構(gòu)組成或配置的差異,不同型號(hào)主要功能的差異應(yīng)當(dāng)包括適應(yīng)證及治療組織位點(diǎn)�。
(二)安全和性能的基本原則
應(yīng)明確申報(bào)產(chǎn)品對(duì)《醫(yī)療器械安全和性能的基本原則》(附件1)中各項(xiàng)要求的適用性。對(duì)于不適用的要求��,應(yīng)當(dāng)逐項(xiàng)說(shuō)明不適用的理由��。對(duì)于適用要求�,應(yīng)逐項(xiàng)說(shuō)明為符合要求所采用的方法,以及證明其符合性的文件��。關(guān)于證明各項(xiàng)要求符合性的文件���,如果包含在產(chǎn)品注冊(cè)申報(bào)資料中�,應(yīng)當(dāng)說(shuō)明其在申報(bào)資料中的具體位置�。對(duì)于未包含在產(chǎn)品注冊(cè)申報(bào)資料中的文件,應(yīng)當(dāng)注明該證據(jù)文件名稱及其在質(zhì)量管理體系文件中的編號(hào)備查��。證明各項(xiàng)要求符合性的文件舉例:風(fēng)險(xiǎn)分析報(bào)告第6章質(zhì)量管理體系文件《產(chǎn)品防護(hù)控制程序》。
(三)綜述資料
1.工作原理
根據(jù)產(chǎn)品自身結(jié)構(gòu)特點(diǎn)闡述各關(guān)鍵組件的工作原理�。例如,激光發(fā)生的原理��、光束傳輸及控制的原理�,可根據(jù)產(chǎn)品實(shí)際研發(fā)情況進(jìn)行描述,明確激光的工作物質(zhì)和激光放大方式�。可結(jié)合光凝機(jī)結(jié)構(gòu)圖和配合不同應(yīng)用部件的光路圖進(jìn)行說(shuō)明�。如有多個(gè)波長(zhǎng),需分別描述各波長(zhǎng)的激光發(fā)生原理及輸出方式�。舉例見附件2。
2.作用機(jī)理
應(yīng)詳述產(chǎn)品發(fā)生的激光與生物組織相互作用(明確作用的色基)的機(jī)理���。應(yīng)當(dāng)分別描述不同波長(zhǎng)���、不同激光輸出方式(工作模式)下作用于何種靶組織,采用了何種能量參數(shù)范圍��,滿足了什么樣的臨床需求��,可治療什么樣的疾?。ㄟm應(yīng)證)��。
3.適用范圍和禁忌證
不同波長(zhǎng)的激光應(yīng)分別描述適用范圍/適應(yīng)證。如:在醫(yī)療機(jī)構(gòu)中使用���,532nm及659nm可用于視網(wǎng)膜光凝���;577nm可用于視網(wǎng)膜和脈絡(luò)膜血管和結(jié)構(gòu)異常的視網(wǎng)膜光凝。視網(wǎng)膜光凝的適應(yīng)證包括增殖型和嚴(yán)重非增殖型糖尿病視網(wǎng)膜病變��、脈絡(luò)膜新生血管�、視網(wǎng)膜靜脈阻塞、年齡相關(guān)性黃斑變性�、視網(wǎng)膜撕裂和脫離、早產(chǎn)兒視網(wǎng)膜病變等���。
禁忌證應(yīng)說(shuō)明光凝機(jī)不適宜應(yīng)用的某些疾病�、情況或特定的人群��。例如�,全視網(wǎng)膜光凝的禁忌證包括角膜感染性炎癥、嚴(yán)重的葡萄膜炎合并滲出�、屈光間質(zhì)混濁不能看清視網(wǎng)膜等。光凝治療的禁忌證包括禁忌黃斑拱環(huán)內(nèi)(直徑500μm)病灶光凝治療�、近視性脈絡(luò)膜新生血管的光凝治療等。
4.與其他同類產(chǎn)品的區(qū)別
應(yīng)提供同品種對(duì)比產(chǎn)品(在國(guó)、內(nèi)外已上市產(chǎn)品)或前代產(chǎn)品的信息��,并闡述申請(qǐng)注冊(cè)的產(chǎn)品開發(fā)的背景和目的�。對(duì)于同類產(chǎn)品研究開發(fā)所參照的理由。描述產(chǎn)品有哪些改進(jìn)�,改進(jìn)的意義是什么,解決了哪些技術(shù)問(wèn)題或臨床問(wèn)題��。同時(shí)���,在對(duì)比表中需說(shuō)明申請(qǐng)注冊(cè)產(chǎn)品和參照產(chǎn)品在工作原理�、作用機(jī)理�、結(jié)構(gòu)組成、性能指標(biāo)以及適用范圍等方面的異同�。
5.包裝說(shuō)明
提供整機(jī)的外包裝及內(nèi)部各組件的包裝情況。如產(chǎn)品組成中包含一次性使用無(wú)菌附件(如眼內(nèi)光纖)�,則提供該附件與滅菌方法相適應(yīng)的最初包裝的信息。
6.明確與其配合使用的裝置
光凝機(jī)配合不同應(yīng)用部件��,如裂隙燈顯微鏡適配器���、眼內(nèi)光纖�、全視網(wǎng)膜光凝適配器��、多點(diǎn)掃描適配器等�,應(yīng)說(shuō)明其連接方式,提供配合使用裝置的相關(guān)信息���,如生產(chǎn)企業(yè)��、型號(hào)���、注冊(cè)證書(如有)。
(四)非臨床資料
1.產(chǎn)品風(fēng)險(xiǎn)分析
眼科激光光凝機(jī)主要的風(fēng)險(xiǎn)包括能量危害��、生物學(xué)危害��、環(huán)境危害��、與使用有關(guān)的危害��、功能失效及老化有關(guān)的危害等��,可參考YY/T 0316的條款對(duì)每種可能涉及的危害識(shí)別評(píng)估���,形成風(fēng)險(xiǎn)分析管理報(bào)告�。舉例見附件3��。
2.產(chǎn)品性能研究
應(yīng)明確所采用的標(biāo)準(zhǔn)或方法、采用的原因及理論基礎(chǔ)�。結(jié)合產(chǎn)品的作用機(jī)理詳述性能指標(biāo)(如功率/能量、脈寬��、重復(fù)頻率等)確定的依據(jù)��,并提供各激光輸出方式(脈沖��、脈沖串等)的波形圖�。研究資料中性能、功能指標(biāo)的確定依據(jù)應(yīng)明確��,不能籠統(tǒng)地描述為“依據(jù)同類產(chǎn)品特點(diǎn)”��、“依據(jù)產(chǎn)品的臨床需求確定”��,應(yīng)說(shuō)明是產(chǎn)品的什么特點(diǎn)��,何種臨床需求���。對(duì)于參考同類產(chǎn)品確定的��,應(yīng)提供同類產(chǎn)品的相關(guān)資料�。適用的國(guó)家標(biāo)準(zhǔn)��、行業(yè)標(biāo)準(zhǔn)中,如果有不適用的條款�,也應(yīng)將不適用的條款及理由予以說(shuō)明。對(duì)于依據(jù)國(guó)家標(biāo)準(zhǔn)�、行業(yè)標(biāo)準(zhǔn)設(shè)定的指標(biāo)��,如性能參數(shù)可參考YY 1289��,應(yīng)關(guān)注標(biāo)準(zhǔn)中是否給出了具體的數(shù)值�,對(duì)于未給出具體要求的,應(yīng)說(shuō)明申報(bào)產(chǎn)品性能指標(biāo)確定的依據(jù)�。對(duì)于特殊功能,應(yīng)詳細(xì)說(shuō)明工作原理和作用機(jī)理并提交相應(yīng)的驗(yàn)證資料�。如產(chǎn)品組成中包含透鏡,則應(yīng)明確透鏡對(duì)申報(bào)產(chǎn)品輸出中心波長(zhǎng)的透過(guò)率���,并提交支持性資料��。
光凝機(jī)的關(guān)鍵性能參數(shù)應(yīng)能反映技術(shù)特征并在產(chǎn)品技術(shù)要求中體現(xiàn)���,至少包括峰值波長(zhǎng)、光束發(fā)散角(或會(huì)聚角)��、光斑尺寸�、脈沖功率/能量范圍���、激光輸出方式、脈沖特性等��;掃描功能(若有)應(yīng)給出掃描參數(shù)��,至少包括:掃描圖形及排列方式、圖形尺寸、光斑尺寸��、掃描次數(shù)、點(diǎn)個(gè)數(shù)�、點(diǎn)間隙等;若光凝機(jī)以脈沖串的方式進(jìn)行輸出�,還應(yīng)給出子脈沖寬度和間隔的設(shè)定依據(jù)。
還應(yīng)詳述產(chǎn)品調(diào)節(jié)能量的方式���,如調(diào)節(jié)能量還是調(diào)節(jié)脈寬或調(diào)節(jié)功率��。若是調(diào)節(jié)脈寬或功率���,提供詳細(xì)對(duì)應(yīng)數(shù)據(jù)表(不同能量下的脈寬和功率)。如果能量參數(shù)相比已上市的產(chǎn)品做出改進(jìn),應(yīng)詳細(xì)說(shuō)明改進(jìn)是如何實(shí)現(xiàn)的���。是通過(guò)設(shè)計(jì)改進(jìn)�、關(guān)鍵元器件更換、還是因?yàn)樯a(chǎn)工藝改進(jìn)或試驗(yàn)方法更改���、軟件調(diào)節(jié)激光輸出方式等���。
區(qū)別于同類產(chǎn)品的特征是技術(shù)審評(píng)關(guān)注的重點(diǎn),除了描述能量參數(shù)的設(shè)置(功率或能量��、脈寬��、重復(fù)頻率等)�,產(chǎn)品調(diào)節(jié)能量的方式(調(diào)脈寬還是調(diào)頻率)���,脈沖特征��,還應(yīng)提交激光脈沖形成機(jī)制(軟件調(diào)�、開關(guān)調(diào)��、Q開關(guān)的光電器件調(diào)等)��,波形實(shí)測(cè)圖���、光束質(zhì)量(光斑均勻性��、光斑能量分布圖���、光斑圖形)等研究資料���。
3.生物相容性評(píng)價(jià)研究
生物相容性評(píng)價(jià)可根據(jù)GB/T 16886.1和《關(guān)于印發(fā)醫(yī)療器械生物學(xué)評(píng)價(jià)和審評(píng)指南的通知》的要求進(jìn)行。應(yīng)對(duì)產(chǎn)品各結(jié)構(gòu)組成(如:主機(jī)��、激光應(yīng)用部件(如眼內(nèi)光纖/裂隙燈顯微鏡/裂隙燈適配器/間接檢眼鏡���、激光防護(hù)眼鏡等)與患者和使用者接觸部分的生物相容性進(jìn)行評(píng)價(jià)�。應(yīng)以列表的形式明確各部位材質(zhì)(包括名稱\牌號(hào)\結(jié)構(gòu)式\分子式等)��。如應(yīng)用新材料���,建議詳述其理化性能和生物學(xué)特性�。如在說(shuō)明書中明確“使用者需佩戴手套操作���、患者需使用墊紙等”��,可不對(duì)接觸部分進(jìn)行生物相容性評(píng)價(jià)���??蓞⒖肌夺t(yī)用激光光纖產(chǎn)品注冊(cè)技術(shù)審查指導(dǎo)原則》��、《裂隙燈顯微鏡注冊(cè)技術(shù)審查指導(dǎo)原則》中的相關(guān)要求�。眼內(nèi)激光光纖若開展生物學(xué)試驗(yàn)的應(yīng)考慮評(píng)價(jià)眼刺激。
4.清洗消毒滅菌工藝研究
光凝機(jī)的主機(jī)��、裂隙燈顯微鏡��、激光防護(hù)眼鏡�、間接檢眼鏡等若涉及終端用戶消毒及滅菌,制造商應(yīng)當(dāng)明確推薦的消毒及滅菌工藝(方法和參數(shù))以及所推薦消毒及滅菌方法確定的依據(jù)��。
眼內(nèi)激光光纖一般應(yīng)為一次性使用無(wú)菌產(chǎn)品�,應(yīng)明確是生產(chǎn)企業(yè)滅菌后交付還是用戶滅菌�。應(yīng)明確滅菌工藝(方法和參數(shù))和無(wú)菌保證水平,并提供滅菌確認(rèn)報(bào)告���。對(duì)于采用輻照滅菌的��,應(yīng)當(dāng)提供最大可接受劑量�、滅菌劑量以及劑量分布的研究�。如果滅菌使用的方法容易出現(xiàn)殘留,應(yīng)當(dāng)明確殘留物的信息及采取的處理方法���,并提供研究資料���。
5.產(chǎn)品有效期及包裝研究
光凝機(jī)的主機(jī)���、裂隙燈顯微鏡、激光防護(hù)眼鏡��、間接檢眼鏡等使用期限一般主要取決于使用過(guò)程中部件及元器件的損耗��、老化等���,應(yīng)按照聲稱的使用期限進(jìn)行老化/疲勞試驗(yàn)���,也可對(duì)影響設(shè)備使用期限的關(guān)鍵部件進(jìn)行老化/疲勞試驗(yàn),例如設(shè)備中不可更換(或更換成本高)的部件��,并提供相應(yīng)的研究資料��。研究資料應(yīng)能證明上述部件按照所聲稱的使用期限��,經(jīng)過(guò)老化/疲勞試驗(yàn)后���,產(chǎn)品性能和安全仍符合預(yù)期的要求�。使用期限也可基于已有數(shù)據(jù)進(jìn)行合理的推斷、分析���、計(jì)算得出�,但應(yīng)提供詳細(xì)的說(shuō)明及支持性資料���??蓞⒖肌队性瘁t(yī)療器械使用期限注冊(cè)技術(shù)審查指導(dǎo)原則》的要求��。
無(wú)菌包裝的眼內(nèi)激光光纖��,可參照YY/T 0681.1��、YY/T 0681.2���、YY/T 0681.3、YY/T 0681.4的條款提交貨架有效期和包裝研究資料���,不同包裝的產(chǎn)品需分別提供��。貨架有效期的研究資料應(yīng)當(dāng)能證明在有效期內(nèi)光纖的安全有效性���。
注冊(cè)申請(qǐng)人應(yīng)結(jié)合聲稱的儲(chǔ)運(yùn)條件開展包裝和環(huán)境試驗(yàn)研究�,并論述研究設(shè)置的合理性��?��?蓞⒖枷嚓P(guān)標(biāo)準(zhǔn)進(jìn)行論述��,例如GB/T14710��。應(yīng)模擬在貯存和運(yùn)輸過(guò)程中的情形開展研究��,證明產(chǎn)品在所聲稱的儲(chǔ)運(yùn)條件下不會(huì)發(fā)生性能��、功能改變���,包裝系統(tǒng)具有保護(hù)產(chǎn)品的能力。經(jīng)過(guò)模擬試驗(yàn)后���,觀察包裝外觀是否有不可接受的異?�,F(xiàn)象���,對(duì)產(chǎn)品進(jìn)行性能測(cè)試�,證明運(yùn)輸和環(huán)境測(cè)試后產(chǎn)品能夠保持其完整性和功能性���。
6.軟件及網(wǎng)絡(luò)安全研究
產(chǎn)品結(jié)構(gòu)組成中若包含作為醫(yī)療器械組成部分(嵌入式軟件和/或獨(dú)立軟件)的軟件���,應(yīng)按照《醫(yī)療器械軟件注冊(cè)技術(shù)審查指導(dǎo)原則》的要求提供一份單獨(dú)的醫(yī)療器械軟件描述文檔,內(nèi)容包括基本信息�、實(shí)現(xiàn)過(guò)程和核心算法三部分內(nèi)容,詳盡程度取決于軟件的安全性級(jí)別和復(fù)雜程度���。同時(shí)��,應(yīng)出具關(guān)于軟件版本命名規(guī)則的聲明,并明確軟件完整版本的全部字段及字段含義�,確定軟件的完整版本和發(fā)行所用的標(biāo)識(shí)版本�。
產(chǎn)品若符合《醫(yī)療器械網(wǎng)絡(luò)安全注冊(cè)技術(shù)審查指導(dǎo)原則》中的適用情形�,應(yīng)提交網(wǎng)絡(luò)安全描述文檔��,并在產(chǎn)品技術(shù)要求中規(guī)定相應(yīng)的性能指標(biāo)。
7.其他安全有效性的研究資料
對(duì)于臨床醫(yī)生來(lái)講��,在一定條件下��,若凝固同一組織的能量恒定,功率提高�,手術(shù)時(shí)間減少�,手術(shù)效率會(huì)提高。由于眼內(nèi)各組織厚度值較低���,尤其是視網(wǎng)膜組織�,功率提高也許會(huì)傷害視神經(jīng)細(xì)胞,增加視野范圍減小�、視功能減退的風(fēng)險(xiǎn)�;若調(diào)整脈寬���、脈沖間隔,延長(zhǎng)手術(shù)時(shí)間��,會(huì)導(dǎo)致熱能量累積�,增加傳導(dǎo)至周邊組織的風(fēng)險(xiǎn),也會(huì)影響視野范圍���、視功能。因此�,應(yīng)當(dāng)提交量效關(guān)系及熱損傷的研究資料�。
量效關(guān)系及熱損傷研究應(yīng)為申報(bào)產(chǎn)品臨床前的體內(nèi)外試驗(yàn)(離體及在體的動(dòng)物試驗(yàn)��、臺(tái)架試驗(yàn)等)�、臨床試驗(yàn)等一項(xiàng)或多項(xiàng)研究所獲得數(shù)據(jù)的分析和總結(jié)。至少應(yīng)評(píng)價(jià)光凝機(jī)在不同波長(zhǎng)下的各種工作模式���、激光輸出方式等對(duì)臨床使用(應(yīng)包括各種適應(yīng)證或各種類型的組織)的影響,并提交研究報(bào)告���。應(yīng)在使用說(shuō)明書中給出相關(guān)的信息���,如梯度功率與光凝組織厚度的量效關(guān)系�。
8.動(dòng)物試驗(yàn)
8.1決策開展動(dòng)物試驗(yàn)
可參考《醫(yī)療器械動(dòng)物試驗(yàn)研究技術(shù)審查指導(dǎo)原則第一部分:決策原則》���。在申報(bào)產(chǎn)品的研發(fā)早期,設(shè)計(jì)輸入及輸出的階段時(shí)�,為降低注冊(cè)申請(qǐng)人研究負(fù)擔(dān)�,激光產(chǎn)品的性能評(píng)估(光凝效率、熱損傷范圍)可選擇臺(tái)架試驗(yàn)或離體組織試驗(yàn)���。如已有上述情形的初步研究或證據(jù)時(shí),也可直接開展動(dòng)物試驗(yàn)研究��。當(dāng)體外試驗(yàn)不能充分評(píng)估光凝機(jī)在臨床應(yīng)用中的安全有效性的風(fēng)險(xiǎn)時(shí)�,需要開展體內(nèi)動(dòng)物試驗(yàn)。通過(guò)體內(nèi)動(dòng)物試驗(yàn)可以更客觀�、完整的提供支持光凝機(jī)作用于眼內(nèi)組織的可行性��、安全性的證據(jù)��。
應(yīng)當(dāng)對(duì)申報(bào)產(chǎn)品能量參數(shù)的設(shè)置、激光與靶組織的作用機(jī)理��、適用范圍及適應(yīng)證等因素進(jìn)行綜合考量�,結(jié)合已有的研究或證據(jù)��,開展適當(dāng)?shù)娘L(fēng)險(xiǎn)分析評(píng)估后�,決策是否需要開展動(dòng)物試驗(yàn)���。決策時(shí)至少應(yīng)當(dāng)評(píng)估以下幾種情形:
8.1.1相比于已上市的產(chǎn)品,選擇一種新的激光波長(zhǎng)作用于原適用范圍中的靶組織(視網(wǎng)膜)�。例如:已上市的產(chǎn)品中�,激光器波長(zhǎng)設(shè)置為綠光采用532nm或黃光采用577nm或紅光采用659 nm�、810nm��,而申報(bào)產(chǎn)品采用一種全新的波長(zhǎng)的情況��;
8.1.2相比于已上市的產(chǎn)品�,選擇一種新的激光作用機(jī)理作用于原適用范圍中的靶組織。例如:申報(bào)產(chǎn)品的輸出方式是通過(guò)軟件控制調(diào)制出閾值下的脈沖波實(shí)現(xiàn)生物刺激效應(yīng)��,而已上市產(chǎn)品采用的是連續(xù)波及脈沖波的情況;
8.1.3相比于已上市的產(chǎn)品,選擇一種新的能量參數(shù)范圍作用于原適用范圍中的靶組織�,如申報(bào)產(chǎn)品設(shè)置的治療參數(shù)(功率或能量、脈寬�、脈沖間隔、光斑大小等)與已上市產(chǎn)品有明顯差異���,可能引發(fā)新的安全性風(fēng)險(xiǎn)的情形�。
對(duì)于風(fēng)險(xiǎn)評(píng)估后決策需要開展動(dòng)物試驗(yàn)的情況,若需要開展臨床試驗(yàn)�,動(dòng)物試驗(yàn)應(yīng)在臨床試驗(yàn)前完成���。動(dòng)物試驗(yàn)可以為臨床試驗(yàn)的方案提供依據(jù)���,預(yù)測(cè)在臨床試驗(yàn)中可能出現(xiàn)的不良事件��,降低臨床試驗(yàn)受試者和臨床使用者承擔(dān)的風(fēng)險(xiǎn)��。動(dòng)物試驗(yàn)還可作為臨床評(píng)價(jià)的重要資料。
8.2動(dòng)物試驗(yàn)類型及目的
應(yīng)能反映光凝機(jī)不同波長(zhǎng)下的各種工作模式或激光輸出方式與臨床應(yīng)用的量效關(guān)系及熱損傷情況���,應(yīng)包括驗(yàn)證申報(bào)產(chǎn)品不同能量參數(shù)對(duì)視網(wǎng)膜光凝及周邊非治療區(qū)域熱擴(kuò)散情況�,且研究結(jié)果應(yīng)能用于評(píng)價(jià)申報(bào)產(chǎn)品的可行性、安全性��。
建議詳細(xì)說(shuō)明選擇試驗(yàn)動(dòng)物模型的依據(jù)���。動(dòng)物數(shù)量可按照試驗(yàn)設(shè)計(jì)需求自行設(shè)定。如選擇的動(dòng)物模型對(duì)于產(chǎn)品應(yīng)用于人體的安全有效性分析具有局限性��,應(yīng)對(duì)研究結(jié)果的影響進(jìn)行詳細(xì)說(shuō)明��。
動(dòng)物試驗(yàn)應(yīng)能觀察到產(chǎn)品作用于動(dòng)物之前���、之后不同時(shí)間點(diǎn)的組織狀態(tài),研究中應(yīng)選擇的觀察時(shí)間點(diǎn)���,應(yīng)有合理依據(jù)�。由于動(dòng)物模型和人體之間組織損傷與愈合應(yīng)答存在差異以及不同激光產(chǎn)品能量參數(shù)設(shè)置存在差異性�,因此本指導(dǎo)原則推薦用于評(píng)估安全性的最終觀察時(shí)間點(diǎn)僅供參考。
建議考慮對(duì)產(chǎn)品不同模式下的能量參數(shù)包括功率或能量�、光斑大小、脈寬及脈沖間隔(若有)等關(guān)鍵性能參數(shù)進(jìn)行評(píng)價(jià)���,且結(jié)果應(yīng)能滿足臨床使用需求�。
推薦術(shù)前、術(shù)后對(duì)組織狀態(tài)進(jìn)行影像學(xué)評(píng)估���,如光學(xué)相干斷層掃描(OCT)檢查或組織病理學(xué)評(píng)估���。
試驗(yàn)研究中,建議盡可能對(duì)臨床相關(guān)的安全性事件進(jìn)行觀察���,如視網(wǎng)膜前和視網(wǎng)膜下纖維化/增殖�、脈絡(luò)膜新生血管形成�、視網(wǎng)膜水腫、視網(wǎng)膜穿孔等��。
動(dòng)物試驗(yàn)舉例詳見附件4�。
9.產(chǎn)品技術(shù)要求
應(yīng)按照《醫(yī)療器械產(chǎn)品技術(shù)要求編寫指導(dǎo)原則》編寫產(chǎn)品技術(shù)要求結(jié)合激光產(chǎn)品的特點(diǎn)設(shè)置條款,存在多種型號(hào)的��,應(yīng)明確不同型號(hào)之間的異同�。若含有軟件,應(yīng)明確軟件發(fā)布版本和軟件完整版本號(hào)的命名規(guī)則���。
性能指標(biāo)中須對(duì)激光輸出特性參數(shù)做出要求�,對(duì)與光凝機(jī)配合使用的各附件分別做出要求,還應(yīng)給出軟件功能���、網(wǎng)絡(luò)安全、環(huán)境適應(yīng)性和安全的要求�。激光性能參數(shù)可參照YY 1289的適用條款進(jìn)行要求,若包含圖形掃描功能��,還應(yīng)制定:掃描圖形���、圖形尺寸�、光斑尺寸��、掃描次數(shù)��、點(diǎn)個(gè)數(shù)�、點(diǎn)間隙等掃描參數(shù);若脈沖串包含子脈沖�,還應(yīng)制定脈沖串寬度、脈沖串間隔�、子脈沖寬度、子脈沖間隔等參數(shù)�。
配合使用的附件可根據(jù)申報(bào)的適用性做出相應(yīng)要求,如光纖可參照YY/T 0758�,裂隙燈顯微鏡可參照YY 0065,間接檢眼鏡可參照YY 0633的要求制定。腳踏開關(guān)應(yīng)符合YY 1057的要求���;激光防護(hù)鏡上應(yīng)標(biāo)明防護(hù)的波長(zhǎng)(或波長(zhǎng)范圍)��,可見光透射比≥30%��;光密度值≥4�。
軟件功能及網(wǎng)絡(luò)安全可根據(jù)產(chǎn)品的實(shí)際情況編寫�。如軟件功能包括數(shù)據(jù)導(dǎo)出功能、視頻或圖像的記錄功能等��。網(wǎng)絡(luò)安全功能給出:數(shù)據(jù)接口��、存儲(chǔ)格式和傳輸協(xié)議���、用戶訪問(wèn)控制程序���、軟件更新的程序等。
此外�,還應(yīng)注意控制裂隙燈顯微鏡及目鏡處激光輻射保證反射或透射至醫(yī)生處的能量在安全范圍內(nèi),應(yīng)參照行標(biāo)合理設(shè)置激光器的峰值波長(zhǎng)允差范圍��,應(yīng)給出各激光輸出方式下的波形實(shí)測(cè)圖��。
10.檢驗(yàn)報(bào)告
檢驗(yàn)產(chǎn)品典型性:原則上,同一注冊(cè)單元選擇結(jié)構(gòu)最復(fù)雜�、功能最多、技術(shù)指標(biāo)最高的型號(hào)進(jìn)行性能和電氣安全檢測(cè)��。如果檢測(cè)一個(gè)型號(hào)不能覆蓋其他型號(hào)的全部性能功能�,則可對(duì)其他型號(hào)不能覆蓋的部分進(jìn)行差異檢測(cè)。EMC檢測(cè)如有典型型號(hào)覆蓋的應(yīng)當(dāng)由檢測(cè)機(jī)構(gòu)出具相關(guān)文件���。技術(shù)審評(píng)重點(diǎn)關(guān)注檢測(cè)內(nèi)容是否與產(chǎn)品技術(shù)要求一致,應(yīng)包括所有的產(chǎn)品結(jié)構(gòu)組成���。
(五)臨床評(píng)價(jià)資料
光凝機(jī)不屬于列入《免于臨床評(píng)價(jià)醫(yī)療器械目錄》中的產(chǎn)品���,應(yīng)當(dāng)依據(jù)所申報(bào)產(chǎn)品的結(jié)構(gòu)組成、性能參數(shù)和預(yù)期用途等��,按照《醫(yī)療器械臨床評(píng)價(jià)技術(shù)指導(dǎo)原則》的要求�,提供相應(yīng)的臨床評(píng)價(jià)資料。
(六)產(chǎn)品說(shuō)明書和標(biāo)簽樣稿
產(chǎn)品說(shuō)明書和標(biāo)簽應(yīng)符合《醫(yī)療器械說(shuō)明書和標(biāo)簽管理規(guī)定》��、GB9706.1�、GB7247.1、GB9706.20��、YY0505中有關(guān)產(chǎn)品使用說(shuō)明書及標(biāo)簽的相關(guān)要求。說(shuō)明書至少應(yīng)包含以下內(nèi)容:產(chǎn)品型號(hào)規(guī)格及功能���;產(chǎn)品的適用范圍及適應(yīng)證�、禁忌證�、不良反應(yīng)/副作用;產(chǎn)品安裝和使用說(shuō)明或者圖示�;符合ISO15004的相關(guān)內(nèi)容(若適用);設(shè)備的基本參數(shù)相關(guān)內(nèi)容應(yīng)與產(chǎn)品技術(shù)要求���、檢驗(yàn)報(bào)告等其他注冊(cè)資料一致��;生產(chǎn)日期���,使用期限或者失效日期、運(yùn)輸���、儲(chǔ)存條件��。適應(yīng)證應(yīng)明確具體的術(shù)式或疾病��,如:中心性漿液性脈絡(luò)膜視網(wǎng)膜病變�,視網(wǎng)膜分支靜脈阻塞/視網(wǎng)膜中央靜脈阻塞引起的黃斑水腫��,脈絡(luò)膜新生血管。應(yīng)當(dāng)明確產(chǎn)品在醫(yī)療機(jī)構(gòu)使用��;應(yīng)明確目標(biāo)用戶及其操作該產(chǎn)品應(yīng)當(dāng)具備的技能/知識(shí)/培訓(xùn)��。
警告及注意事項(xiàng)至少包括:使用資質(zhì)的要求��,如只能由經(jīng)過(guò)培訓(xùn)的專業(yè)的醫(yī)務(wù)人員操作���;電磁兼容方面相關(guān)的警告及措施��;不應(yīng)放置在影響本產(chǎn)品運(yùn)行和性能的位置的警告;應(yīng)給出清洗���、消毒��、滅菌的說(shuō)明���;對(duì)于一次性使用的附件或部件,應(yīng)有不可重復(fù)使用的警告�;對(duì)檢修人員、銷售商及相關(guān)人員���,應(yīng)提供說(shuō)明如何檢修產(chǎn)品的調(diào)整裝置及其工作過(guò)程��。應(yīng)提示治療光束對(duì)周邊人員造成潛在的能量危害并提供相應(yīng)的防護(hù)措施��。
標(biāo)簽應(yīng)當(dāng)符合《醫(yī)療器械說(shuō)明書和標(biāo)簽管理規(guī)定》���。醫(yī)療器械標(biāo)簽因位置或者大小受限而無(wú)法全部標(biāo)明上述內(nèi)容的��,至少應(yīng)當(dāng)標(biāo)注產(chǎn)品名稱��、型號(hào)��、規(guī)格��、生產(chǎn)日期和使用期限或者失效日期,并在標(biāo)簽中明確“其他內(nèi)容詳見說(shuō)明書”��。
三��、參考文獻(xiàn)
[1] Peng Q, Juzeniene A, Chen J Y, et al. Lasers in medicine [J]. Reports on Progress in Physics, 2008, 71(5): 1–28.
[2] 國(guó)家食品藥品監(jiān)督管理總局關(guān)于發(fā)布醫(yī)療器械分類目錄的公告(2017年第104號(hào)) [EB/OL]. https://www. nmpa.gov. cn/ylqx/lqxggtg/ylqxqtgg/20170904150301537.html
[3] 國(guó)家藥品監(jiān)督管理局關(guān)于發(fā)布醫(yī)療器械動(dòng)物試驗(yàn)研究注冊(cè)審查指導(dǎo)原則 第一部分:決策原則(2021年修訂版)等2項(xiàng)注冊(cè)審查指導(dǎo)原則的通告(2021年第75號(hào))[EB/OL]. https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20210927153130147.html?type=pc&m=
附件:1. 醫(yī)療器械安全和性能的基本原則舉例
2. 眼科激光光凝機(jī)的工作原理及作用機(jī)理
3. 眼科激光光凝機(jī)風(fēng)險(xiǎn)分析資料要求
4. 動(dòng)物試驗(yàn)舉例
附件1
醫(yī)療器械安全和性能的基本原則舉例
條款號(hào) | 要求 | 適用性判斷 |
1. | 醫(yī)療器械的安全和性能—總則 |
注冊(cè)人/備案人的設(shè)計(jì)和生產(chǎn)活動(dòng)應(yīng)在質(zhì)量管理體系的控制下進(jìn)行���。注冊(cè)人/備案人應(yīng)提供產(chǎn)品與適用基本原則條款符合的證據(jù)��,并由監(jiān)管機(jī)構(gòu)按照相關(guān)程序進(jìn)行評(píng)審。 | 適用 |
2. | 適用于所有醫(yī)療器械的通用基本原則 |
本部分所列設(shè)計(jì)和生產(chǎn)通用基本原則適用于所有醫(yī)療器械��。 |
2.1 | 概述 |
|
2.1.1 | 醫(yī)療器械應(yīng)實(shí)現(xiàn)注冊(cè)人/備案人的預(yù)期性能,其設(shè)計(jì)和生產(chǎn)應(yīng)確保器械在預(yù)期使用條件下達(dá)到預(yù)期目的��。這些器械應(yīng)是安全的并且能夠?qū)崿F(xiàn)其預(yù)期性能����,與患者受益相比�����,其風(fēng)險(xiǎn)應(yīng)是可接受的���,且不會(huì)損害醫(yī)療環(huán)境�、患者安全�、使用者及他人的安全和健康。 | 適用 |
2.1.2 | 注冊(cè)人/備案人應(yīng)建立�����、實(shí)施�����、形成文件和維護(hù)風(fēng)險(xiǎn)管理體系���,確保醫(yī)療器械安全��、有效且質(zhì)量可控�。在醫(yī)療器械全生命周期內(nèi)�����,風(fēng)險(xiǎn)管理是一個(gè)持續(xù)�����、反復(fù)的過(guò)程��,需要定期進(jìn)行系統(tǒng)性的改進(jìn)更新��。在開展風(fēng)險(xiǎn)管理時(shí)�,注冊(cè)人/備案人應(yīng): a) 建立涵蓋所有醫(yī)療器械風(fēng)險(xiǎn)管理計(jì)劃并形成文件���; b) 識(shí)別并分析涵蓋所有醫(yī)療器械的相關(guān)的已知和可預(yù)見的危險(xiǎn)(源)�; c) 估計(jì)和評(píng)價(jià)在預(yù)期使用和可合理預(yù)見的誤使用過(guò)程中���,發(fā)生的相關(guān)風(fēng)險(xiǎn)�; d) 依據(jù)2.1.3和2.1.4相關(guān)要求,消除或控制c)點(diǎn)所述的風(fēng)險(xiǎn)���; e) 評(píng)價(jià)生產(chǎn)和生產(chǎn)后階段信息對(duì)綜合風(fēng)險(xiǎn)��、風(fēng)險(xiǎn)受益判定和風(fēng)險(xiǎn)可接受性的影響�����。上述評(píng)價(jià)應(yīng)包括先前未識(shí)別的危險(xiǎn)(源)或危險(xiǎn)情況���,由危險(xiǎn)情況導(dǎo)致的一個(gè)或多個(gè)風(fēng)險(xiǎn)對(duì)可接受性的影響,以及對(duì)先進(jìn)技術(shù)水平的改變等�����。 f) 基于對(duì)e)點(diǎn)所述信息影響的評(píng)價(jià)���,必要時(shí)修改控制措施以符合2.1.3和2.1.4相關(guān)要求��。 | 適用 |
2.1.3 | 醫(yī)療器械的注冊(cè)人/備案人在設(shè)計(jì)和生產(chǎn)過(guò)程中采取的風(fēng)險(xiǎn)控制措施,應(yīng)遵循安全原則��,采用先進(jìn)技術(shù)�����。需要降低風(fēng)險(xiǎn)時(shí),注冊(cè)人/備案人應(yīng)控制風(fēng)險(xiǎn)���,確保每個(gè)危險(xiǎn)(源)相關(guān)的剩余風(fēng)險(xiǎn)和總體剩余風(fēng)險(xiǎn)是可接受的�。在選擇最合適的解決方案時(shí)���,注冊(cè)人/備案人應(yīng)按以下優(yōu)先順序進(jìn)行: a) 通過(guò)安全設(shè)計(jì)和生產(chǎn)消除或適當(dāng)降低風(fēng)險(xiǎn)�; b) 適用時(shí)�����,對(duì)無(wú)法消除的風(fēng)險(xiǎn)采取充分的防護(hù)措施���,包括必要的警報(bào)���; c) 提供安全信息(警告/預(yù)防措施/禁忌證),適當(dāng)時(shí)���,向使用者提供培訓(xùn)���。 | 適用 |
2.1.4 | 注冊(cè)人/備案人應(yīng)告知使用者所有相關(guān)的剩余風(fēng)險(xiǎn)��。 | 適用 |
2.1.5 | 在消除或降低與使用有關(guān)的風(fēng)險(xiǎn)時(shí)����,注冊(cè)人/備案人應(yīng)該: a) 適當(dāng)降低醫(yī)療器械的特性(如人體工程學(xué)/可用性)和預(yù)期使用環(huán)境(如灰塵和濕度)可能帶來(lái)的風(fēng)險(xiǎn)��; b) 考慮預(yù)期使用者的技術(shù)知識(shí)��、經(jīng)驗(yàn)��、教育背景�、培訓(xùn)、身體狀況(如適用)以及使用環(huán)境�。 | 適用 |
2.1.6 | 在注冊(cè)人/備案人規(guī)定的生命周期內(nèi),在正常使用���、維護(hù)和校準(zhǔn)(如適用)情況下�����,外力不應(yīng)對(duì)醫(yī)療器械的特性和性能造成不利影響�����,以致?lián)p害患者、使用者及他人的健康和安全。 | 適用 |
2.1.7 | 醫(yī)療器械的設(shè)計(jì)�、生產(chǎn)和包裝,包括注冊(cè)人/備案人所提供的說(shuō)明和信息���,應(yīng)確保在按照預(yù)期用途使用時(shí)��,運(yùn)輸和貯存條件(例如:震動(dòng)�����、振動(dòng)�、溫度和濕度的波動(dòng))不會(huì)對(duì)醫(yī)療器械的特性和性能�,包括完整性和清潔度,造成不利影響�����。注冊(cè)人/備案人應(yīng)能確保有效期內(nèi)醫(yī)療器械的性能�、安全和無(wú)菌保證水平。 | 適用 |
2.1.8 | 在貨架有效期內(nèi)��、開封后的使用期間(對(duì)于體外診斷試劑�,包括在機(jī)(機(jī)載)穩(wěn)定性),以及運(yùn)輸或送貨期間(對(duì)于體外診斷試劑��,包括樣品),醫(yī)療器械應(yīng)具有可接受的穩(wěn)定性��。 | 適用 |
2.1.9 | 在正常使用條件下�����,基于當(dāng)前先進(jìn)技術(shù)水平���,比較醫(yī)療器械性能帶來(lái)的受益���,所有已知的、可預(yù)見的風(fēng)險(xiǎn)以及任何不良副作用應(yīng)最小化且可接受���。 | 適用 |
2.2 | 臨床評(píng)價(jià) |
2.2.1 | 基于監(jiān)管要求���,醫(yī)療器械可能需要進(jìn)行臨床評(píng)價(jià)(如適用)。所謂臨床評(píng)價(jià)�����,就是對(duì)臨床數(shù)據(jù)進(jìn)行評(píng)估��,確定醫(yī)療器械具有可接受的風(fēng)險(xiǎn)受益比���,包括以下幾種形式: a) 臨床試驗(yàn)報(bào)告 b) 臨床文獻(xiàn)資料 c) 臨床經(jīng)驗(yàn)數(shù)據(jù) | 適用 |
2.2.2 | 臨床試驗(yàn)的實(shí)施應(yīng)符合《赫爾辛基宣言》的倫理原則���。 保護(hù)受試者的權(quán)利、安全和健康�,作為最重要的考慮因素,其重要性超過(guò)科學(xué)和社會(huì)效益�����。在臨床試驗(yàn)的每個(gè)步驟���,都應(yīng)理解����、遵守和使用上述原則�。另外,臨床試驗(yàn)方案審批�����、患者知情同意���、體外診斷試劑剩余樣本使用等應(yīng)符合相關(guān)法規(guī)要求����。 | 適用 |
2.3 | 化學(xué)、物理和生物學(xué)特性 |
2.3.1 | 關(guān)于醫(yī)療器械的化學(xué)���、物理和生物學(xué)特性����,應(yīng)特別注意以下幾點(diǎn): a) 所用材料和組成成分的選擇�����,需特別考慮: -毒性�; -生物相容性; -易燃性���; b) 工藝對(duì)材料性能的影響����; c) 生物物理學(xué)或者建模研究結(jié)果應(yīng)事先進(jìn)行驗(yàn)證(如適用)���; d) 所用材料的機(jī)械性能���,如適用����,應(yīng)考慮強(qiáng)度��、延展性�、斷裂強(qiáng)度、耐磨性和抗疲勞性等屬性��; e) 表面特性�; f) 器械與已規(guī)定化學(xué)和/或物理性能的符合性�����。 | 適用 |
2.3.2 | 基于醫(yī)療器械的預(yù)期用途�,醫(yī)療器械的設(shè)計(jì)、生產(chǎn)和包裝����,應(yīng)盡可能減少污染物和殘留物對(duì)使用者和患者,以及對(duì)從事醫(yī)療器械運(yùn)輸�����、貯存及其他相關(guān)人員造成的風(fēng)險(xiǎn)�����。特別要注意與使用者和患者暴露組織接觸的時(shí)間和頻次。 | 適用 |
2.3.3 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)適當(dāng)降低析出物(包括濾瀝物和/或蒸發(fā)物)�����、降解產(chǎn)物���、加工殘留物等造成的風(fēng)險(xiǎn)��。應(yīng)特別注意致癌���、致突變或有生殖毒性的泄漏物或?yàn)V瀝物。 | 不適用 |
2.3.4 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)考慮到醫(yī)療器械及其預(yù)期使用環(huán)境的性質(zhì)�,適當(dāng)降低物質(zhì)意外進(jìn)入器械所帶來(lái)的風(fēng)險(xiǎn)。 | 適用 |
2.3.5 | 醫(yī)療器械及其生產(chǎn)工藝的設(shè)計(jì)應(yīng)能消除或適當(dāng)降低對(duì)使用者和其他可能接觸者的感染風(fēng)險(xiǎn)��。設(shè)計(jì)應(yīng): a) 操作安全����,易于處理; b) 盡量減少醫(yī)療器械的微生物泄漏和/或使用過(guò)程中的感染風(fēng)險(xiǎn)�����; c) 防止醫(yī)療器械或其內(nèi)容物(例如:標(biāo)本)的微生物污染; d) 盡量減少意外風(fēng)險(xiǎn)(例如:割傷和刺傷(如針刺傷)��、意外物質(zhì)濺入眼睛等)���。 | 適用 |
2.4 | 滅菌和微生物污染 |
2.4.1 | 醫(yī)療器械其設(shè)計(jì)應(yīng)方便使用者對(duì)其進(jìn)行安全清潔����、消毒���、滅菌和/或重復(fù)滅菌(必要時(shí))。 | 適用 |
2.4.2 | 具有微生物限度要求的醫(yī)療器械��,其設(shè)計(jì)�����、生產(chǎn)和包裝應(yīng)確保在出廠后�,按照注冊(cè)人/備案人規(guī)定的條件運(yùn)輸和貯存,符合微生物限度要求��。 | 適用 |
2.4.3 | 以無(wú)菌狀態(tài)交付的醫(yī)療器械����,其設(shè)計(jì)�、生產(chǎn)和包裝應(yīng)按照適當(dāng)?shù)某绦蜻M(jìn)行��,以確保在出廠時(shí)無(wú)菌�����。在注冊(cè)人/備案人規(guī)定的條件下運(yùn)輸和貯存的未破損無(wú)菌包裝�����,打開前都應(yīng)保持無(wú)菌狀態(tài)�����。應(yīng)確保最終使用者可清晰地辨識(shí)包裝的完整性(例如:防篡改包裝)��。 | 適用 |
2.4.4 | 無(wú)菌醫(yī)療器械應(yīng)按照經(jīng)驗(yàn)證的方法進(jìn)行加工��、生產(chǎn)�����、包裝和滅菌�����,其貨架有效期應(yīng)按照經(jīng)驗(yàn)證的方法確定。 | 適用 |
2.4.5 | 預(yù)期無(wú)菌使用的醫(yī)療器械(注冊(cè)人/備案人滅菌或使用者滅菌)���,均應(yīng)在適當(dāng)且受控的條件和設(shè)施下生產(chǎn)和包裝�。 | 適用 |
2.4.6 | 以非無(wú)菌狀態(tài)交付�,且使用前滅菌的醫(yī)療器械: a) 包裝應(yīng)當(dāng)盡量減少產(chǎn)品受到微生物污染的風(fēng)險(xiǎn),且應(yīng)適用于注冊(cè)人/備案人規(guī)定的滅菌方法�; b) 注冊(cè)人/備案人規(guī)定的滅菌方法應(yīng)經(jīng)過(guò)驗(yàn)證。 | 適用 |
2.4.7 | 若醫(yī)療器械可以無(wú)菌和非無(wú)菌狀態(tài)交付使用��,應(yīng)明確標(biāo)識(shí)其交付狀態(tài)�。 | 適用 |
2.5 | 環(huán)境和使用條件 |
2.5.1 | 如醫(yī)療器械預(yù)期與其他醫(yī)療器械或設(shè)備整合使用,應(yīng)確保整合使用后的系統(tǒng)���,包括連接系統(tǒng),整體的安全性��,且不影響器械本身的性能�����。整合使用上的限制應(yīng)明確標(biāo)識(shí)和/或在使用說(shuō)明書中明確�。對(duì)于需要使用者處理的連接�����,如液體��、氣體傳輸�����、電耦合或機(jī)械耦合等���,在設(shè)計(jì)和生產(chǎn)過(guò)程中盡可能消除或降低所有可能的風(fēng)險(xiǎn),包括錯(cuò)誤連接或安全危害�。 | 適用 |
2.5.2 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)考慮預(yù)期的使用環(huán)境和使用條件,以消除或降低下列風(fēng)險(xiǎn): | / |
a) 與物理和人體工程學(xué)/可用性的特性有關(guān)�,對(duì)使用者或他人造成損傷的風(fēng)險(xiǎn); | 適用 |
b) 由于用戶界面設(shè)計(jì)�、人體工程學(xué)/可用性的特性以及預(yù)期使用環(huán)境導(dǎo)致的錯(cuò)誤操作的風(fēng)險(xiǎn); | 適用 |
c) 與合理可預(yù)期的外部因素或環(huán)境條件有關(guān)的風(fēng)險(xiǎn)��,如磁場(chǎng)���、外部電磁效應(yīng)���、靜電釋放�、診斷和治療帶來(lái)的輻射�、壓力、濕度����、溫度和/或壓力和加速度的變化; | 適用 |
d) 正常使用條件下與固體材料��、液體和其他物質(zhì)�����,包括氣體���,接觸而產(chǎn)生的風(fēng)險(xiǎn)�����; | 不適用 |
e) 軟件與信息技術(shù)(IT)運(yùn)行環(huán)境的兼容性造成的風(fēng)險(xiǎn)�; | 適用 |
f) 正常使用過(guò)程中���,醫(yī)療器械非預(yù)期析出物導(dǎo)致的環(huán)境風(fēng)險(xiǎn); | 適用 |
g) 樣本/樣品/數(shù)據(jù)不正確識(shí)別和錯(cuò)誤結(jié)果導(dǎo)致的風(fēng)險(xiǎn)��,比如用于分析、測(cè)試或檢測(cè)的樣本容器�、可拆卸部件和/或附件,其顏色和/或數(shù)字編碼混淆����; | 不適用 |
h) 與其他用于診斷、監(jiān)測(cè)或治療的醫(yī)療器械互相干擾導(dǎo)致的風(fēng)險(xiǎn)����。 | 適用 |
2.5.3 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)消除或降低在正常狀態(tài)及單一故障狀態(tài)下燃燒和爆炸的風(fēng)險(xiǎn),尤其是預(yù)期用途包括暴露于易燃��、易爆物質(zhì)或其他可致燃物相關(guān)的器械聯(lián)用�。 | 適用 |
2.5.4 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)能確保調(diào)整、校準(zhǔn)和維護(hù)過(guò)程能夠安全有效的完成�����。 | 適用 |
a) 對(duì)無(wú)法進(jìn)行維護(hù)的醫(yī)療器械��,如植入物�����,應(yīng)盡量降低材料老化等風(fēng)險(xiǎn)��; | 不適用 |
b) 對(duì)無(wú)法進(jìn)行調(diào)整和校準(zhǔn)的醫(yī)療器械,如某些類型的溫度計(jì)�����,應(yīng)盡量降低測(cè)量或控制機(jī)制精度的損失風(fēng)險(xiǎn)�����。 | 不適用 |
2.5.5 | 與其他醫(yī)療器械或產(chǎn)品聯(lián)合使用的醫(yī)療器械�����,其設(shè)計(jì)和生產(chǎn)應(yīng)能保證互操作性和兼容性可靠且安全����。 | 適用 |
2.5.6 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)能降低未經(jīng)授權(quán)的訪問(wèn)風(fēng)險(xiǎn), 這種訪問(wèn)可能會(huì)妨礙器械正常運(yùn)行�,或造成安全隱患。 | 適用 |
2.5.7 | 具有測(cè)量��、監(jiān)視或有數(shù)值顯示功能的醫(yī)療器械�,其設(shè)計(jì)和生產(chǎn)應(yīng)符合人體工程學(xué)/可用性原則,并應(yīng)顧及器械預(yù)期用途�、預(yù)期使用者、使用環(huán)境。 | 適用 |
2.5.8 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)便于使用者����、患者或其他人員對(duì)其以及相關(guān)廢棄物的安全處置或再利用�����。使用說(shuō)明書應(yīng)明確安全處置或回收的程序和方法���。 | 適用 |
2.6 | 對(duì)電氣�����、機(jī)械和熱風(fēng)險(xiǎn)的防護(hù) |
2.6.1 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)具有機(jī)械相關(guān)的防護(hù),保護(hù)使用者免于承受由諸如運(yùn)動(dòng)阻力、不穩(wěn)定性和活動(dòng)部件等引起的機(jī)械風(fēng)險(xiǎn)�����。 | 適用 |
2.6.2 | 除非振動(dòng)是器械特定性能的一部分�,否則醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)將產(chǎn)品振動(dòng)導(dǎo)致的風(fēng)險(xiǎn)降到最低,應(yīng)盡量采用限制振動(dòng)(特別是振動(dòng)源)的方法����。 | 適用 |
2.6.3 | 除非噪聲是器械特定性能的一部分,否則醫(yī)療器械設(shè)計(jì)和生產(chǎn)應(yīng)將產(chǎn)品噪聲導(dǎo)致的風(fēng)險(xiǎn)降到最低,應(yīng)盡量采用限制噪聲(特別是噪聲源)的方法�。 | 適用 |
2.6.4 | 如果醫(yī)療器械的部件在使用前或使用中需要進(jìn)行連接或重新連接,其設(shè)計(jì)和生產(chǎn)應(yīng)降低這些部件間的連接故障風(fēng)險(xiǎn)����。 | 適用 |
2.6.5 | 醫(yī)療器械的可接觸部件(不包括用于供熱或既定溫度設(shè)置部位)及其周圍環(huán)境,在正常使用時(shí)不應(yīng)存在過(guò)熱風(fēng)險(xiǎn)����。 | 適用 |
2.7 | 有源醫(yī)療器械及與其連接的醫(yī)療器械 |
2.7.1 | 當(dāng)有源醫(yī)療器械發(fā)生單一故障時(shí),應(yīng)采取適當(dāng)?shù)拇胧┫蚪档鸵虼硕a(chǎn)生的風(fēng)險(xiǎn)�。 | 適用 |
2.7.2 | 患者的安全依賴于內(nèi)部電源供電的醫(yī)療器械,應(yīng)具有檢測(cè)供電狀態(tài)的功能����,并在電源容量不足時(shí)提供適當(dāng)?shù)奶崾净蚓妗?/p> | 不適用 |
2.7.3 | 患者的安全取決于外部電源供電狀態(tài)的醫(yī)療器械,應(yīng)包括可顯示任何電源故障的報(bào)警系統(tǒng)����。 | 適用 |
2.7.4 | 用于監(jiān)視患者一個(gè)或多個(gè)臨床指標(biāo)的醫(yī)療器械,必須配備適當(dāng)報(bào)警系統(tǒng)��,在患者健康狀況惡化或危及生命時(shí)����,向使用者發(fā)出警報(bào)。 | 不適用 |
2.7.5 | 鑒于電磁干擾可能會(huì)損害正常運(yùn)行的裝置或設(shè)備,醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)降低產(chǎn)生電磁干擾的風(fēng)險(xiǎn)�����。 | 適用 |
2.7.6 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn)����,應(yīng)確保產(chǎn)品具有足夠的抗電磁干擾能力�,以確保產(chǎn)品的正常運(yùn)行。 | 適用 |
2.7.7 | 當(dāng)產(chǎn)品按注冊(cè)人/備案人的說(shuō)明進(jìn)行安裝和維護(hù)����,在正常狀態(tài)和單一故障狀態(tài)時(shí),醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)減少使用者和他人免于遭受意外電擊的風(fēng)險(xiǎn)�����。 | 適用 |
2.8 | 含有軟件的醫(yī)療器械以及獨(dú)立軟件 |
2.8.1 | 含有電子可編程系統(tǒng)(內(nèi)含軟件組件)的醫(yī)療器械或獨(dú)立軟件的設(shè)計(jì)�,應(yīng)確保準(zhǔn)確度、可靠性���、精確度����、安全和性能符合其預(yù)期用途。應(yīng)采取適當(dāng)措施��,消除或減少單一故障導(dǎo)致的風(fēng)險(xiǎn)或性能降低�。 | 適用 |
2.8.2 | 含有軟件組件的醫(yī)療器械或獨(dú)立軟件,應(yīng)根據(jù)先進(jìn)技術(shù)進(jìn)行開發(fā)�����、生產(chǎn)和維護(hù)�,同時(shí)應(yīng)考慮開發(fā)生存周期(如快速迭代開發(fā)、頻繁更新��、更新的累積效應(yīng))�����、風(fēng)險(xiǎn)管理(如系統(tǒng)��、環(huán)境和數(shù)據(jù)的變化)等原則�����,包括信息安全(如安全地進(jìn)行更新)����、驗(yàn)證和確認(rèn)(如更新管理過(guò)程)的要求��。 | 適用 |
2.8.3 | 預(yù)期與移動(dòng)計(jì)算平臺(tái)整合使用的軟件�����,其設(shè)計(jì)和開發(fā)����,應(yīng)考慮平臺(tái)本身(如屏幕尺寸和對(duì)比度�����、聯(lián)通性�、內(nèi)存等)以及與其使用相關(guān)的外部因素(不同環(huán)境下的照明或噪聲水平)�����。 | 不適用 |
2.8.4 | 注冊(cè)人/備案人應(yīng)規(guī)定軟件按照預(yù)期正常運(yùn)行所必須的最低要求��,如硬件�、IT網(wǎng)絡(luò)特性和IT網(wǎng)絡(luò)安全措施,包括未經(jīng)授權(quán)的訪問(wèn)�。 | 適用 |
2.8.5 | 醫(yī)療器械的設(shè)計(jì)、生產(chǎn)和維護(hù)應(yīng)能提供足夠的網(wǎng)絡(luò)安全水平�����,以防止未經(jīng)授權(quán)的訪問(wèn)。 | 適用 |
2.9 | 具有診斷或測(cè)量功能的醫(yī)療器械 |
2.9.1 | 具有診斷或測(cè)量(包括監(jiān)測(cè))功能的醫(yī)療器械的設(shè)計(jì)和生產(chǎn)����,應(yīng)基于適當(dāng)?shù)目萍挤椒ǎ渌阅芡?����,還應(yīng)確保相應(yīng)的準(zhǔn)確度���、精密度和穩(wěn)定性�,以實(shí)現(xiàn)其預(yù)期目的��。 | 不適用 |
a) 注冊(cè)人/備案人應(yīng)規(guī)定準(zhǔn)確度限值(如適用)��。 | 不適用 |
b) 為便于使用者理解和接受�,數(shù)字化測(cè)量值應(yīng)以標(biāo)準(zhǔn)化單位表示(如可能),推薦使用國(guó)際通用的標(biāo)準(zhǔn)計(jì)量單位���,考慮到安全�、使用者的熟悉程度和既往的臨床實(shí)踐��,也可使用其他公認(rèn)的計(jì)量單位。 | 不適用 |
c) 醫(yī)療器械導(dǎo)示器和控制器的功能應(yīng)有詳細(xì)的說(shuō)明����,若器械通過(guò)可視化系統(tǒng)提供與操作、操作指示或調(diào)整參數(shù)有關(guān)的說(shuō)明�,該類信息應(yīng)能夠被使用者和患者(適用時(shí))理解。 | 不適用 |
2.10 | 說(shuō)明書和標(biāo)簽 |
2.10.1 | 醫(yī)療器械應(yīng)附有識(shí)別該器械及其注冊(cè)人/備案人所需的信息�。每個(gè)醫(yī)療器械還應(yīng)附有相關(guān)安全和性能信息或相關(guān)指示。這些信息可出現(xiàn)在器械本身��、包裝上或使用說(shuō)明書中�,或者可以通過(guò)電子手段(如網(wǎng)站)便捷訪問(wèn),易于被預(yù)期使用者理解��。 | 適用 |
2.11 | 輻射防護(hù) |
2.11.1 | 醫(yī)療器械的設(shè)計(jì)���、生產(chǎn)和包裝應(yīng)當(dāng)考慮盡量減少使用者、他人和患者(如適用)的輻射吸收劑量����,同時(shí)不影響其診斷或治療功能。 | 適用 |
2.11.2 | 具有輻射或潛在輻射危害的醫(yī)療器械�,其操作說(shuō)明應(yīng)詳細(xì)說(shuō)明輻射的性質(zhì),對(duì)使用者����、他人或患者(若適用)的防護(hù)措施��,避免誤用的方法��,降低運(yùn)輸��、貯存和安裝的風(fēng)險(xiǎn)��。 | 適用 |
2.11.3 | 若醫(yī)療器械有輻射或有潛在輻射危害����,應(yīng)具備輻射泄漏聲光報(bào)警功能(如可行)�����。 | 適用 |
2.11.4 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn)應(yīng)降低使用者����、其他人員或患者(若適用)暴露于非預(yù)期、偏離或散射輻射的風(fēng)險(xiǎn)�����。在可能和適當(dāng)?shù)那闆r下�����,應(yīng)采取措施減少使用者、其他人員或患者(若適用)等可能受影響的人在輻射中的暴露�����。 | 適用 |
2.11.5 | 具有輻射或潛在輻射危害且需要安裝的醫(yī)療器械�,應(yīng)在操作說(shuō)明中明確有關(guān)驗(yàn)收和性能測(cè)試、驗(yàn)收標(biāo)準(zhǔn)及維護(hù)程序的信息���。 | 適用 |
2.11.6 | 若醫(yī)療器械對(duì)使用者有輻射或潛在輻射危害�����,其設(shè)計(jì)和生產(chǎn)應(yīng)確保輻射劑量����、幾何分布����、能量分布(或質(zhì)量)以及其他輻射關(guān)鍵特性能夠得到合理的控制和調(diào)整�,并可在使用過(guò)程中進(jìn)行監(jiān)控(如適用)。上述醫(yī)療器械的設(shè)計(jì)和生產(chǎn)����,應(yīng)確保相關(guān)可變參數(shù)的重復(fù)性在可接受范圍內(nèi)�。 | 不適用 |
2.12 | 對(duì)非專業(yè)用戶使用風(fēng)險(xiǎn)的防護(hù) |
2.12.1 | 對(duì)于非專業(yè)用戶使用的醫(yī)療器械(如自測(cè)或近患者檢 測(cè))���,為保證醫(yī)療器械的正常使用�,其設(shè)計(jì)和生產(chǎn)應(yīng)考慮非專業(yè)用戶的操作技能���,以及因非專業(yè)用戶技術(shù)和使用環(huán)境的不同對(duì)結(jié)果的影響�����。注冊(cè)人/備案人提供的信息和說(shuō)明應(yīng)易于理解和使用�,并可對(duì)結(jié)果做出解釋�。 | 不適用 |
2.12.2 | 供非專業(yè)用戶使用的醫(yī)療器械(如自測(cè)或近患者檢測(cè)) 的設(shè)計(jì)和生產(chǎn)應(yīng): a) 確保使用者可以按照使用說(shuō)明書的規(guī)定安全準(zhǔn)確的使用。當(dāng)無(wú)法將與說(shuō)明書相關(guān)的風(fēng)險(xiǎn)降低到適當(dāng)水平時(shí)�����,可以通過(guò)培訓(xùn)來(lái)降低此類風(fēng)險(xiǎn)�����; b) 盡可能減少非專業(yè)用戶因錯(cuò)誤操作和錯(cuò)誤解釋結(jié)果導(dǎo)致的風(fēng)險(xiǎn)。 | 不適用 |
2.12.3 | 供非專業(yè)用戶使用的醫(yī)療器械可通過(guò)以下措施方便用戶: a) 在使用時(shí)�����,可以驗(yàn)證器械的正常運(yùn)行�����; b) 當(dāng)器械不能正常運(yùn)行或提供無(wú)效結(jié)果時(shí)����,會(huì)發(fā)出警告�。 | 不適用 |
2.13 | 含有生物源材料的醫(yī)療器械 |
2.13.1 | 對(duì)于含有動(dòng)植物組織、細(xì)胞或其它物質(zhì)��,細(xì)菌來(lái)源物質(zhì)或衍生物的醫(yī)療器械�,若無(wú)活性或以非活性狀態(tài)交付,應(yīng): a) 組織�、細(xì)胞及其衍生物應(yīng)來(lái)源于已受控且符合預(yù)期用途的動(dòng)物種屬。動(dòng)物的地理來(lái)源信息應(yīng)根據(jù)相關(guān)法規(guī)要求予以保留�����。 b) 動(dòng)物源的組織���、細(xì)胞�����、物質(zhì)或其衍生物的采集��、加工、保存��、檢測(cè)和處理過(guò)程���,應(yīng)確?���;颊?����、使用者以及其他人員(如適用)的安全����。特別是病毒和其他傳染性病原體�,應(yīng)通過(guò)經(jīng)驗(yàn)證的先進(jìn)技術(shù)消除或滅活,影響醫(yī)療器械性能的情況除外�。 | 不適用 |
2.13.2 | 對(duì)于監(jiān)管部門而言���,當(dāng)醫(yī)療器械由人體來(lái)源的組織、細(xì)胞����、物質(zhì)或其衍生物生產(chǎn)時(shí),應(yīng)采取以下措施: a) 組織�、細(xì)胞的捐贈(zèng)、獲取和檢測(cè)應(yīng)依據(jù)相關(guān)法規(guī)的要求進(jìn)行��; b) 為確?�;颊?��、使用者或他人的安全,應(yīng)對(duì)組織��、細(xì)胞或其衍生物進(jìn)行加工�����、保存或其他處理��。對(duì)于病毒和其他傳染源�����,應(yīng)通過(guò)源頭控制����,或在生產(chǎn)過(guò)程中通過(guò)經(jīng)驗(yàn)證的先進(jìn)技術(shù)消除或滅活����。 | 不適用 |
2.13.3 | 當(dāng)醫(yī)療器械使用2.13.1、2.13.2以外的生物物質(zhì)(例如植物或細(xì)菌來(lái)源的材料)生產(chǎn)時(shí)時(shí)�,其加工、保存�、檢測(cè)和處理應(yīng)確保患者�、用戶以及其他人員(如廢棄物處置人員等)的安全。對(duì)于病毒和其他傳染源���,為確保安全���,應(yīng)通過(guò)源頭控制�����,或在生產(chǎn)過(guò)程中通過(guò)經(jīng)驗(yàn)證的先進(jìn)技術(shù)消除或滅活�。 | 不適用 |
3. | 適用于醫(yī)療器械(體外診斷類醫(yī)療器械除外)的基本原則 |
本部分所列設(shè)計(jì)和生產(chǎn)基本原則是第2節(jié)相關(guān)內(nèi)容的補(bǔ)充�,適用于非體外診斷類醫(yī)療器械。 |
3.1 | 化學(xué)��、物理和生物學(xué)特性 |
3.1.1 | 根據(jù)醫(yī)療器械的預(yù)期用途�����,以及產(chǎn)品(例如某些可吸收產(chǎn)品)在人體的吸收��、分布�����、代謝和排泄情況����,對(duì)于醫(yī)療器械的化學(xué)、物理和生物學(xué)特性�,應(yīng)特別注意所用材料/物質(zhì)與人體組織、細(xì)胞和體液之間的相容性��。 | 適用 |
3.1.2 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn),應(yīng)當(dāng)能夠保證產(chǎn)品在預(yù)期使用中接觸到其他的材料��、物質(zhì)和氣體時(shí)����,仍然能夠安全使用����。如果醫(yī)療器械用于配合藥物使用,則該產(chǎn)品的設(shè)計(jì)和生產(chǎn)需要符合藥品管理的有關(guān)規(guī)定����,且具有藥物相容性,同時(shí)藥品和器械的性能符合其適應(yīng)證和預(yù)期用途����。 | 不適用 |
3.1.3 | 醫(yī)療器械的設(shè)計(jì)和生產(chǎn),除接觸完整皮膚的產(chǎn)品外�,應(yīng)適當(dāng)降低釋放進(jìn)入患者或使用者體內(nèi)的顆粒,產(chǎn)生與顆粒尺寸和性質(zhì)相關(guān)的風(fēng)險(xiǎn)�����。對(duì)納米材料應(yīng)給予重點(diǎn)關(guān)注�����。 | 適用 |
3.2 | 輻射防護(hù) |
3.2.1 | 用于醫(yī)學(xué)影像的醫(yī)療器械具有電離輻射時(shí),其設(shè)計(jì)和生產(chǎn)��,在保障圖像和/或輸出質(zhì)量的同時(shí)�,應(yīng)盡可能降低患者、使用者和其他人員的輻射吸收劑量����。 | 不適用 |
3.2.2 | 具有電離輻射的醫(yī)療器械應(yīng)能夠精確預(yù)估(或監(jiān)測(cè))、顯示����、報(bào)告和記錄治療過(guò)程中的輻射劑量。 | 不適用 |
3.3 | 植入醫(yī)療器械的特殊要求 |
3.3.1 | 植入醫(yī)療器械的設(shè)計(jì)和生產(chǎn)�,應(yīng)能消除或降低相關(guān)治療風(fēng)險(xiǎn),例如除顫器��、高頻手術(shù)設(shè)備的使用��。 | 不適用 |
3.3.2 | 可編程有源植入式醫(yī)療器械的設(shè)計(jì)和生產(chǎn)�����,應(yīng)保證產(chǎn)品在無(wú)需手術(shù)時(shí)即可準(zhǔn)確識(shí)別����。 | 不適用 |
3.4 | 提供能量或物質(zhì)的醫(yī)療器械對(duì)患者或使用者的風(fēng)險(xiǎn)防護(hù) |
3.4.1 | 用于給患者提供能量或物質(zhì)的醫(yī)療器械�,其設(shè)計(jì)和生產(chǎn)應(yīng)能精確地設(shè)定和維持輸出量�����,以保證患者����、使用者和其他人的安全。 | 適用 |
3.4.2 | 若輸出量不足可能導(dǎo)致危險(xiǎn)�,醫(yī)療器械應(yīng)當(dāng)具有防止和/或指示“輸出量不足”的功能���。意外輸出危險(xiǎn)等級(jí)量的能量或物質(zhì)作為較大風(fēng)險(xiǎn)����,應(yīng)采取適當(dāng)?shù)拇胧┯枰越档汀?/p> | 適用 |
3.5 | 含有藥物成分的組合產(chǎn)品 |
3.5.1 | 當(dāng)醫(yī)療器械組成成分中含有某種物質(zhì)����,依據(jù)監(jiān)管法規(guī),該物質(zhì)作為藥用產(chǎn)品/藥物進(jìn)行管理�,且該物質(zhì)在體內(nèi)為醫(yī)療器械提供輔助作用時(shí),應(yīng)將醫(yī)療器械和此物質(zhì)作為一個(gè)整體�,對(duì)其安全和性能進(jìn)行驗(yàn)證����,同時(shí)應(yīng)驗(yàn)證該物質(zhì)的特征��、安全��、質(zhì)量和有效性���。 | 不適用 |
附件2
眼科激光光凝機(jī)的工作原理及作用機(jī)理
一����、工作原理
光凝機(jī)一般包括主機(jī)�、激光應(yīng)用部件(如眼內(nèi)光纖、裂隙燈顯微鏡�、裂隙燈適配器、間接檢眼鏡)����、和/或其他輔助設(shè)備,有些是主機(jī)��、激光應(yīng)用部件與裂隙燈顯微鏡集成一體(如圖1所示)�。以半導(dǎo)體泵浦的固體532nm激光為例,說(shuō)明光凝機(jī)激光發(fā)生的原理(如圖2所示),激光二極管發(fā)射泵浦光�,泵浦光經(jīng)過(guò)聚焦準(zhǔn)直后照射至激光工作物質(zhì)(Nd:YVO4),發(fā)生受激輻射后激發(fā)出1064nm光子����;1064nm光子在全反鏡和輸出鏡之間反射,互相之間不斷發(fā)生相干放大形成1064nm激光��;1064nm激光經(jīng)過(guò)倍頻晶體后�,發(fā)生非線性光學(xué)效應(yīng)中的二次諧波效應(yīng),一部分轉(zhuǎn)化為532nm激光�����,透過(guò)輸出鏡形成532nm激光輸出��;532nm激光經(jīng)過(guò)偏振片和分光鏡��,小部分被發(fā)射至能量探測(cè)器��,轉(zhuǎn)化為電信號(hào)反饋至控制及安全電路��,大部分輸出至光纖聚焦鏡��,經(jīng)過(guò)光纖聚焦鏡后���,與調(diào)節(jié)至同光路的瞄準(zhǔn)光�����,一起從激光耦合口輸出(如圖3所示)�,通過(guò)激光應(yīng)用部件���,如眼內(nèi)光纖�����、裂隙燈顯微鏡�����、裂隙燈適配器��、間接檢眼鏡將激光引導(dǎo)到患者眼中��。
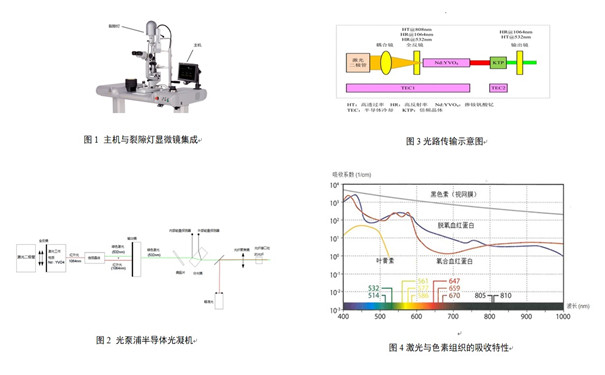
二�����、作用機(jī)理
1.不同波長(zhǎng)的激光會(huì)被眼內(nèi)不同的色素組織吸收�����,如視網(wǎng)膜色素上皮層或脈絡(luò)膜中的黑色素��、血液中的血紅蛋白��、葉黃素等(如圖4所示)���。532nm為綠光�,血紅蛋白和黑色素吸收高�,黃斑區(qū)的葉黃素吸收少,視網(wǎng)膜色素上皮層吸收較多�;560nm、577nm為黃光�����,氧合血紅蛋白吸收率最大����,黑色素吸收少�����,葉黃素吸收相對(duì)較少, 脈絡(luò)膜毛細(xì)血管淺層吸收較多。810nm為近紅外光����,血液中的血紅蛋白吸收較少,光透射率較高�����;與可見光波段相比�����,黑色素吸收較少�,穿透力強(qiáng),脈絡(luò)膜動(dòng)靜脈血管吸收較多而葉黃素幾乎不吸收��。
2.常見的激光與組織的相互作用可分為熱效應(yīng)�����、光化效應(yīng)�、光致爆破效應(yīng)、壓強(qiáng)效應(yīng)和生物刺激效應(yīng)�。當(dāng)激光作用于人體組織時(shí),這些效應(yīng)很多都是同時(shí)發(fā)生的�,并沒有嚴(yán)格的界限����,在一定的條件下��,以某種效應(yīng)為主����。光凝機(jī)涉及的主要包括兩種效應(yīng):
(1)激光熱效應(yīng),組織吸收激光能量后轉(zhuǎn)為熱能�����,激光
能量被視網(wǎng)膜色素上皮層或脈絡(luò)膜中的黑色素和血液中的血紅蛋白吸收并產(chǎn)生熱量��,導(dǎo)致組織溫度升高��,蛋白質(zhì)變性產(chǎn)生凝固現(xiàn)象�。
(2)生物刺激效應(yīng),也稱為光的生物學(xué)效應(yīng)��。低強(qiáng)度激光照射組織�����,可引起部分細(xì)胞因子發(fā)生變化����,達(dá)到刺激部分受體的目的,起到調(diào)節(jié)作用�。
激光器與組織產(chǎn)生不同的效應(yīng)決定不同臨床應(yīng)用情形,如:
視網(wǎng)膜光凝�����,通過(guò)激光的熱效應(yīng)�,針對(duì)視網(wǎng)膜微血管缺血區(qū)或毛細(xì)血管無(wú)灌注區(qū)進(jìn)行治療,阻止眼內(nèi)新生血管的發(fā)生和發(fā)展��,改變視網(wǎng)膜區(qū)域的缺氧狀態(tài)����。可用于治療糖尿病視網(wǎng)膜病變�����、視網(wǎng)膜靜脈阻塞等����。
通過(guò)激光的生物學(xué)刺激效應(yīng),產(chǎn)生“閾值”(激光凝固組織所需的能量的臨界值)下的脈沖波��,作用于視網(wǎng)膜色素上皮層,視網(wǎng)膜色素上皮細(xì)胞產(chǎn)生中等程度損傷���,引起部分因子發(fā)生變化���,如:血管內(nèi)皮生長(zhǎng)因子(VEGF)下調(diào),熱休克蛋白70(HSP70)上調(diào)等�����?���?梢詼p少新生血管及改變血管通透性,用于治療中心性漿液性脈絡(luò)膜視網(wǎng)膜病變�����,糖尿病視網(wǎng)膜病變以及視網(wǎng)膜靜脈阻塞引起的黃斑水腫�。
附件3
眼科激光光凝機(jī)風(fēng)險(xiǎn)分析資料要求
產(chǎn)品風(fēng)險(xiǎn)分析資料是對(duì)產(chǎn)品的風(fēng)險(xiǎn)管理過(guò)程及其評(píng)審的結(jié)果予以記錄所形成的資料。
眼科激光光凝機(jī)的設(shè)計(jì)應(yīng)能夠保證�����,當(dāng)單個(gè)元件、部分發(fā)生故障時(shí)��,不會(huì)引起不能接受的危害�����。應(yīng)對(duì)由單個(gè)故障條件引起的����,并與產(chǎn)品各功能有關(guān)的危害加以識(shí)別���。對(duì)于每種危害���,其產(chǎn)生傷害的可能性都應(yīng)進(jìn)行評(píng)估,要考慮各種危害控制�,以及對(duì)各故障條件引起的傷害可能性進(jìn)行評(píng)估。
一����、 眼科激光光凝機(jī)可能存在的危險(xiǎn)
以下列出了眼科激光光凝機(jī)可能存在的危險(xiǎn)情況,但不受以下危險(xiǎn)的限制:
1.能量危險(xiǎn)
在眼科激光光凝機(jī)的開發(fā)�����、生產(chǎn)和操作使用中��,出現(xiàn)的能量危險(xiǎn),包括電氣危險(xiǎn)���、電場(chǎng)或磁場(chǎng)危險(xiǎn)�、非電離輻射危險(xiǎn)�����、熱能危險(xiǎn)和機(jī)械危險(xiǎn)����。
2.生化危險(xiǎn)
生物相容性問(wèn)題或藥敏物質(zhì)導(dǎo)致患者的傷害。
3.操作危險(xiǎn)
由于隨附資料不全面�、標(biāo)記不充分引起的誤操作導(dǎo)致的危險(xiǎn),也包括設(shè)備功能退化�、治療數(shù)據(jù)錯(cuò)誤、配件安全錯(cuò)誤以及網(wǎng)絡(luò)安全防護(hù)不足等引起的危險(xiǎn)��。
4.信息危險(xiǎn)
由不完整或錯(cuò)誤的標(biāo)記��、說(shuō)明書����、警告說(shuō)明導(dǎo)致的危險(xiǎn),也包括由于安裝說(shuō)明、維修說(shuō)明等資料不足引起的包括設(shè)備培訓(xùn)��、維修服務(wù)相關(guān)的危險(xiǎn)�����。
眼科激光光凝機(jī)常見的危險(xiǎn)示例見下表1:
表1 眼科激光光凝機(jī)常見的危險(xiǎn)示例
危險(xiǎn)分類 | 危險(xiǎn)原因分類 | 危險(xiǎn)示例 |
能量危險(xiǎn) | 電氣危險(xiǎn) | 電源電纜或組件固定不充分 |
機(jī)械強(qiáng)度和絕緣耐熱性不足 |
在設(shè)備使用壽命期間��,活動(dòng)部件的保護(hù)性接地丟失 |
激光輻射引起的系統(tǒng)起火 |
用戶未將設(shè)備連接至適當(dāng)?shù)碾娫聪到y(tǒng) |
漏電危險(xiǎn)����、接地導(dǎo)體電阻過(guò)大 |
使用劣質(zhì)電源線導(dǎo)致電源線損壞 |
導(dǎo)線和連接器意外脫落�,導(dǎo)致在連接電路時(shí)出現(xiàn)危險(xiǎn)情況 |
清潔和消毒過(guò)程中,對(duì)部件(包括應(yīng)用部件和配件)造成損壞 |
未測(cè)試ME系統(tǒng)的結(jié)合使用情況 |
安全關(guān)鍵部件的涂層全部或部分損失 |
激光設(shè)備老化(包括組件和單元)��,導(dǎo)致漏電流過(guò)大 |
供電網(wǎng)電壓波動(dòng)�����,導(dǎo)致供電電壓偏高或偏低 |
元件機(jī)械強(qiáng)度和絕緣耐熱性不足�����,或使用有缺陷的組件 |
電場(chǎng)或磁場(chǎng)危險(xiǎn) | 對(duì)ESD的抵抗力不足�,意外出現(xiàn)激光發(fā)射控制信號(hào) |
對(duì)電快速瞬變的抵抗力不足,意外出現(xiàn)激光發(fā)射控制信號(hào) |
對(duì)射頻電磁場(chǎng)的抵抗力不足,意外出現(xiàn)激光發(fā)射控制信號(hào) |
抗浪涌能力不足����,意外出現(xiàn)激光發(fā)射控制信號(hào) |
抗傳導(dǎo)干擾能力不足,意外出現(xiàn)激光發(fā)射控制信號(hào) |
對(duì)電壓驟降��、中斷和變化的抵抗力不足����,意外出現(xiàn)激光發(fā)射控制信號(hào) |
對(duì)磁場(chǎng)的抵抗力不足,意外出現(xiàn)激光發(fā)射控制信號(hào) |
電磁輻射發(fā)射量過(guò)大����、過(guò)度傳導(dǎo)電磁輻射、諧波電流發(fā)射量過(guò)大����、電壓波動(dòng)和閃變過(guò)大 |
非電離輻射危險(xiǎn) | D/A轉(zhuǎn)換器故障(控制器的目標(biāo)設(shè)置錯(cuò)誤),或探測(cè)器污染導(dǎo)致功率發(fā)射偏離預(yù)設(shè)值 |
光源發(fā)出過(guò)多的紅外輻射 |
錯(cuò)誤釋放工作光束或未成功切斷工作光束����,導(dǎo)致對(duì)眼部產(chǎn)生非預(yù)期輻射 |
瞄準(zhǔn)光束激光輻射過(guò)多或瞄準(zhǔn)光太弱導(dǎo)致無(wú)法辨別 |
激光發(fā)射模式下,通過(guò)觀察光學(xué)器件的輻射過(guò)多�,如未安裝或未提供醫(yī)生安全濾光片 |
外殼破裂,導(dǎo)致發(fā)出激光輻射 |
掃描機(jī)制完全失效��,導(dǎo)致所有光斑都被激光照射在視網(wǎng)膜的一個(gè)點(diǎn)上 |
在超過(guò)100ms的時(shí)間內(nèi),激光發(fā)射功率超出設(shè)定值的兩倍 |
由于功率控制用光電二極管的精度逐漸降低��,因此�,導(dǎo)致用戶設(shè)置的激光功率與發(fā)射參數(shù)不符。 |
變焦鏡頭系統(tǒng)的色差過(guò)大���,導(dǎo)致焦平面(最大能量密度)不在視網(wǎng)膜上 |
機(jī)械裝置/電機(jī)老化��,導(dǎo)致無(wú)法在規(guī)定時(shí)間內(nèi)定位激光發(fā)射圖案 |
眼睛移動(dòng)引起的治療位置變化 |
在治療過(guò)程中����,意外反射進(jìn)入醫(yī)生眼部 |
腳踏線等信號(hào)路徑發(fā)生短路����,或緊急激光終止器發(fā)生故障�����,導(dǎo)致無(wú)法關(guān)閉激光束 |
治療參數(shù)控制系統(tǒng)和監(jiān)控出現(xiàn)故障�,或電子元件故障,如:光學(xué)器件�、激光電源、CPU板LCD屏����、線纜����、光纖����、后面板等,引起的多余輻射 |
處理器系統(tǒng)時(shí)鐘故障導(dǎo)致脈沖持續(xù)時(shí)間過(guò)長(zhǎng) |
光傳感器故障導(dǎo)致治療激光設(shè)備意外產(chǎn)生輻射 |
熱能危險(xiǎn) | 設(shè)備超溫��,無(wú)防火措施 |
ME設(shè)備的防火外殼不能承受火災(zāi) |
過(guò)電流引起火災(zāi) |
管狀加熱元件引起的危險(xiǎn) |
由于過(guò)量使用設(shè)備導(dǎo)致的系統(tǒng)過(guò)熱 |
機(jī)械危險(xiǎn) | 眼科光凝機(jī)支撐系統(tǒng)不足 |
激光設(shè)備外殼強(qiáng)度不足 |
手機(jī)和腳踏式控制設(shè)備機(jī)械強(qiáng)度不足 |
活動(dòng)部件壓住身體部位 |
用于患者支撐或固定的固定裝置意外松動(dòng) |
機(jī)械保護(hù)裝置設(shè)計(jì)不恰當(dāng) |
系統(tǒng)在不適當(dāng)?shù)沫h(huán)境條件中振動(dòng)����、碰撞 |
未按規(guī)定搬運(yùn)(如運(yùn)輸)有關(guān)的危險(xiǎn),如無(wú)合適的可用包裝 |
聲能 | 激光發(fā)射指示器的聲能過(guò)多���,操作員或患者位置附近的噪音量過(guò)大 |
生化危險(xiǎn) | 毒性物質(zhì)和化學(xué)物質(zhì) | 光纖材質(zhì)毒性或受污染����,使患者受感染 |
光纖接觸人體�����,光纖材質(zhì)可能含毒性物質(zhì) |
接觸可能變脆的表面材料 |
患者/用戶/第三方接觸應(yīng)用部件��,如接觸鏡 |
滅菌與熱原 | 光纖滅菌不當(dāng),滅菌方法選擇不當(dāng)��、光纖污染�,造成患者細(xì)菌感染或者交叉干擾 |
光纖有熱原導(dǎo)致與人體接觸時(shí)產(chǎn)生熱原反應(yīng) |
生物相容性 | 設(shè)備各部件(包括外殼、關(guān)鍵按鈕��、應(yīng)用部分等)與人體接觸部位生物不相容����,造成患者致敏、刺激或者皮內(nèi)反應(yīng) |
操作危險(xiǎn) | 更換組件不當(dāng) | 碰觸高溫表面 |
環(huán)境污染 |
更換時(shí)使用錯(cuò)誤的部件或損壞設(shè)備 |
由未經(jīng)授權(quán)人員進(jìn)行更換 |
維修不當(dāng) | 維護(hù)期間激光功率測(cè)量不足或錯(cuò)誤 |
在維修檢查/維護(hù)過(guò)程中對(duì)設(shè)備的操作錯(cuò)誤���,導(dǎo)致電氣安全不足 |
維修人員未充分接受培訓(xùn)�����,維修期間出現(xiàn)的電氣和光輻射危險(xiǎn) |
維修期間使用的外接軟件工具,可能導(dǎo)致系統(tǒng)的失靈 |
操作不當(dāng) | 預(yù)期用途錯(cuò)誤識(shí)別導(dǎo)致的誤用系統(tǒng) |
治療區(qū)域和靶組織錯(cuò)誤識(shí)別導(dǎo)致患者組織受到嚴(yán)重?fù)p傷 |
錯(cuò)誤理解功能模式設(shè)置或錯(cuò)誤定義治療區(qū)域 |
意外踩下激光腳踏開關(guān)或信號(hào)路徑發(fā)生短路�����,導(dǎo)致激活激光發(fā)射 |
意外調(diào)整激光功率��,輻射過(guò)多的激光能量 |
液體滲透防護(hù)措施不足�,造成激光輻射傷害 |
未充分選擇治療參數(shù)��,導(dǎo)致出現(xiàn)各種并發(fā)癥 |
由于控制元件指示不足���,導(dǎo)致使用了不良的治療參數(shù) |
意外拆卸激光設(shè)備外殼,對(duì)眼部產(chǎn)生非預(yù)期輻射 |
醫(yī)師將在未充分采取輻射防護(hù)措施的情況下開始進(jìn)行治療 |
醫(yī)生定位錯(cuò)誤����,導(dǎo)致眼部組織損傷 |
醫(yī)生意外激活觸發(fā),導(dǎo)致治療激光的非預(yù)期輻射 |
光纖過(guò)度彎曲導(dǎo)致斷裂����,引發(fā)非預(yù)期輻射 |
由于錯(cuò)誤或未校準(zhǔn)的掃描機(jī)制,導(dǎo)致未達(dá)到指定的激光發(fā)射圖案精度(距離)��。 |
在旋轉(zhuǎn)裝置時(shí)�,用戶將該旋轉(zhuǎn)裝置握得太靠近車軸。用戶的手部可能會(huì)受到擠壓傷害 |
用戶界面復(fù)雜或混亂�����,導(dǎo)致操作錯(cuò)誤 |
光纖安裝錯(cuò)誤����,導(dǎo)致治療激光設(shè)備意外產(chǎn)生輻射 |
用戶不了解激光設(shè)備安全激活情況 |
用戶不了解工作條件導(dǎo)致的適用錯(cuò)誤 |
由不符合設(shè)備操作資格的人員進(jìn)行操作,導(dǎo)致操作出現(xiàn)錯(cuò)誤���。 |
操作人員未按照官方安裝說(shuō)明的工作流程進(jìn)行操作���,導(dǎo)致操作錯(cuò)誤�����。 |
在規(guī)定的環(huán)境條件之外進(jìn)行設(shè)備存放�、運(yùn)輸和操作 |
超過(guò)設(shè)備使用壽命后未經(jīng)評(píng)價(jià)繼續(xù)使用 |
網(wǎng)絡(luò)安全引發(fā)的危險(xiǎn) | 未經(jīng)授權(quán)的人員通過(guò)遠(yuǎn)程服務(wù)查看和更改患者數(shù)據(jù) |
未經(jīng)授權(quán)人員濫用患者數(shù)據(jù) |
用戶配置文件無(wú)密碼保護(hù)�,無(wú)意或隨意變更設(shè)備基本設(shè)置 |
用戶配置文件無(wú)密碼保護(hù),不同的用戶可以同時(shí)訪問(wèn)同一數(shù)據(jù) |
缺少不活動(dòng)時(shí)自動(dòng)注銷用戶功能 |
連接局域網(wǎng)時(shí)�����,未采取任何軟件防護(hù)措施 |
對(duì)設(shè)備使用未經(jīng)授權(quán)的軟件���,導(dǎo)致信息丟失 |
應(yīng)用軟件感染了病毒�,無(wú)法獲取患者數(shù)據(jù) |
持續(xù)治療期間的遠(yuǎn)程服務(wù)��,不可預(yù)見的設(shè)備行為 |
信息危險(xiǎn) | 標(biāo)識(shí)�����、標(biāo)志不足引起的危險(xiǎn) | 對(duì)眼部照明源產(chǎn)生的光輻射危險(xiǎn)指示不足 |
激光輻射開關(guān)相關(guān)的標(biāo)識(shí)不足 |
激光輻射標(biāo)記錯(cuò)誤 |
設(shè)備上的警告提示不再清晰�,或用戶手冊(cè)缺失或內(nèi)容不完整,導(dǎo)致接觸帶電部件 |
說(shuō)明書內(nèi)容不足引起的危險(xiǎn) | 用戶手冊(cè)無(wú)有關(guān)組件����、附件的使用說(shuō)明 |
有關(guān)EMC環(huán)境的信息不充分 |
用戶手冊(cè)無(wú)關(guān)于本產(chǎn)品與附件結(jié)合使用時(shí)所帶來(lái)的風(fēng)險(xiǎn)信息 |
無(wú)有關(guān)警告(錯(cuò)誤)更換部件危險(xiǎn)警告 |
用戶手冊(cè)和維修手冊(cè)均未包含性能規(guī)格,導(dǎo)致設(shè)備維修不當(dāng) |
使用說(shuō)明書中缺少有關(guān)采取預(yù)防措施����,防止對(duì)患者、用戶或第三方造成傷害或損害的信息�����。 |
二��、風(fēng)險(xiǎn)分析
風(fēng)險(xiǎn)分析包括醫(yī)療器械適用范圍與安全性有關(guān)特征的判定����、危害的判定、估計(jì)每個(gè)危險(xiǎn)情況的風(fēng)險(xiǎn)�。風(fēng)險(xiǎn)分析過(guò)程中要考慮正常使用條件下和非正常使用條件下合理的可預(yù)見的情況。
下表2為眼科激光光凝機(jī)常見危害�����、可預(yù)見的事件序列、危害處境和損害之間的關(guān)系舉例����。
表2 眼科激光光凝機(jī)危害、可預(yù)見的事件序列����、
危害處境和損害之間的關(guān)系示例
危害 | 可預(yù)見的事件序列 | 危害處境 | 損害 |
能量危害 | 1) 電氣危害,包括:線纜固定不充分�;設(shè)備材料絕緣強(qiáng)度不足;電源系統(tǒng)連接錯(cuò)誤���;生產(chǎn)資料缺陷造成的危害����;元器件連接脫落�;設(shè)備及附件配合使用的電氣危險(xiǎn)增加;關(guān)鍵件涂層脫落��;設(shè)備老化等����。 2) 電磁場(chǎng)危害,包括:電磁場(chǎng)抗干擾能力不足�;電磁輻射發(fā)射過(guò)大等����。 3) 光輻射危害,包括:光源輻射能量過(guò)大;非預(yù)期光譜輻射能量過(guò)大����;瞄準(zhǔn)光輻射過(guò)大或過(guò)低;激光功率波動(dòng)�����;操作不當(dāng)或防護(hù)不當(dāng)��;輻射監(jiān)控模塊故障燈����。 4) 熱能危害,包括:設(shè)備由于過(guò)度使用造成過(guò)熱����;加熱元件引發(fā);過(guò)電流引發(fā)�;無(wú)防火措施或防水外殼不能承受火災(zāi)等。 5) 機(jī)械危害����,包括:患者支撐系統(tǒng)不足�����;設(shè)備及附件強(qiáng)度不足����;活動(dòng)部件對(duì)患者的壓力多大�;機(jī)械保護(hù)裝置設(shè)計(jì)不當(dāng);系統(tǒng)的振動(dòng)��、碰撞等���。 6) 聲能危害��,包括:激光發(fā)射提示音多大等�。 | 1) 增加電氣安全風(fēng)險(xiǎn) 2) 增加非預(yù)期輻射發(fā)射風(fēng)險(xiǎn) 3) 降低設(shè)備的使用壽命 4) 激光輻射或設(shè)備過(guò)熱引發(fā)火災(zāi) 5) 機(jī)械危害對(duì)患者帶來(lái)的碰撞�、擠壓等 | 可能對(duì)操作者、患者帶來(lái)電氣傷害����;同時(shí),產(chǎn)生財(cái)產(chǎn)損失 |
生化危害 | 1) 毒性物質(zhì)和化學(xué)物質(zhì)��,包括:光纖材質(zhì)毒性或污染;表面材料含有化學(xué)物質(zhì)��;可接觸的應(yīng)用部件表面含有化學(xué)物質(zhì)���。 2) 滅菌和熱原,包括:光纖滅菌不當(dāng)��,導(dǎo)致光纖污染�;光纖與人體接觸時(shí)產(chǎn)生的熱原反應(yīng)。 3) 設(shè)備各部件與人體接觸時(shí)生物不相容造成的患者致敏�����、刺激或皮內(nèi)反映����。 | 1) 應(yīng)用部件污染 2) 設(shè)備表面污染 | 導(dǎo)致患者的交叉感染;灼傷患者�,給患者帶來(lái)永久性的傷害 |
操作危害 | 1) 由于操作不當(dāng)引起的危害,包括:意外激發(fā)激光輸出��;意外調(diào)整輸出量的設(shè)置���;選擇治療參數(shù)錯(cuò)誤����;操作者防護(hù)措施不達(dá)標(biāo);設(shè)備附件的不恰當(dāng)使用�����;附件安裝錯(cuò)誤���;操作者未按照設(shè)備程序進(jìn)行操作�;由不符合操作資格的人員進(jìn)行操作等����。 2) 更換組件帶來(lái)的危害,包括:操作不當(dāng)�;處理更換組件不當(dāng);錯(cuò)誤更換�����;未經(jīng)授權(quán)人員進(jìn)行更換等�����。 3) 維修工具不當(dāng)����,包括:維修期間使用的操作工具�、外接軟件工具��,而導(dǎo)致的設(shè)備或軟件失靈���。 4) 網(wǎng)絡(luò)安全危害��,包括:用戶文件無(wú)密碼保護(hù);用戶權(quán)限可任意使用�;應(yīng)用軟件無(wú)防護(hù)措施;軟件感染病毒�;使用未經(jīng)授權(quán)的軟件;遠(yuǎn)程服務(wù)的不受控制�;濫用患者數(shù)據(jù)等。 | 1) 增加操作者和患者的電氣安全風(fēng)險(xiǎn)和光輻射風(fēng)險(xiǎn)��; 2) 降低設(shè)備使用壽命�; 3) 損壞設(shè)備部件; 4) 泄露患者隱私����; 5) 增加治療數(shù)據(jù)丟失的風(fēng)險(xiǎn) | 可能對(duì)操作者、患者帶來(lái)電氣傷害和過(guò)量的光輻射傷害�����;同時(shí),產(chǎn)生財(cái)產(chǎn)損失 |
信息危害 | 1) 信息不全或錯(cuò)誤����,包括:光輻射指示不足;激光輻射相關(guān)標(biāo)識(shí)不足或錯(cuò)誤����;警告提醒不清晰;用戶手冊(cè)缺少安全使用說(shuō)明���、使用環(huán)境說(shuō)明�、預(yù)防措施說(shuō)明等內(nèi)容����。 2) 維修培訓(xùn)不足,包括:維護(hù)期間對(duì)激光輸出量的測(cè)試錯(cuò)誤�����;對(duì)設(shè)備的操作錯(cuò)誤�����;維修人員未接受充分培訓(xùn)等。 | 1) 增加治療參數(shù)設(shè)定錯(cuò)誤風(fēng)險(xiǎn)��; 2) 增加操作者和患者的電氣安全風(fēng)險(xiǎn)和光輻射風(fēng)險(xiǎn)�����; 3) 降低設(shè)備使用壽命�; | 可能患者產(chǎn)生非預(yù)期光輻射,或輻射能量不恰當(dāng)影響臨床��;同時(shí)�����,產(chǎn)生財(cái)產(chǎn)損失 |
|
|
|
|
|
三���、風(fēng)險(xiǎn)評(píng)價(jià)
對(duì)每個(gè)已判定的危害處境,注冊(cè)申請(qǐng)人應(yīng)依據(jù)風(fēng)險(xiǎn)管理計(jì)劃中制定的風(fēng)險(xiǎn)可接受準(zhǔn)則進(jìn)行風(fēng)險(xiǎn)評(píng)價(jià)����,決定是否需要降低風(fēng)險(xiǎn)。風(fēng)險(xiǎn)評(píng)價(jià)的結(jié)果記入風(fēng)險(xiǎn)管理文件中�。
四、風(fēng)險(xiǎn)控制
注冊(cè)申請(qǐng)人應(yīng)對(duì)經(jīng)風(fēng)險(xiǎn)評(píng)價(jià)后不可接受的或考慮可進(jìn)一步采取措施降低的風(fēng)險(xiǎn)制定適當(dāng)?shù)娘L(fēng)險(xiǎn)控制措施(一個(gè)或多個(gè))�����,把風(fēng)險(xiǎn)降低到可接受的水平。在制定降低風(fēng)險(xiǎn)的控制措施方案時(shí)�,應(yīng)充分考慮產(chǎn)品國(guó)家標(biāo)準(zhǔn)、行業(yè)標(biāo)準(zhǔn)中有關(guān)降低風(fēng)險(xiǎn)的措施�����。應(yīng)確保降低風(fēng)險(xiǎn)的控制措施在研制初期得到有效的輸入�,對(duì)每項(xiàng)風(fēng)險(xiǎn)控制措施實(shí)施予以驗(yàn)證,并應(yīng)對(duì)措施的有效性實(shí)施驗(yàn)證��。注冊(cè)申請(qǐng)人應(yīng)對(duì)采取降低風(fēng)險(xiǎn)的控制措施后的剩余風(fēng)險(xiǎn)以及是否會(huì)引發(fā)新的風(fēng)險(xiǎn)進(jìn)行評(píng)價(jià)�����。以上降低風(fēng)險(xiǎn)的控制措施��、控制措施的驗(yàn)證�、剩余風(fēng)險(xiǎn)評(píng)價(jià)等信息可以記入風(fēng)險(xiǎn)管理報(bào)告中。
五�����、綜合剩余風(fēng)險(xiǎn)的可接受性評(píng)價(jià)
注冊(cè)申請(qǐng)人應(yīng)對(duì)綜合剩余風(fēng)險(xiǎn)是否可接受給出結(jié)論性意見,并對(duì)運(yùn)用恰當(dāng)?shù)姆椒ǐ@得與本產(chǎn)品相關(guān)的生產(chǎn)信息與臨床應(yīng)用的信息進(jìn)行闡述并做出承諾�。
風(fēng)險(xiǎn)管理報(bào)告應(yīng)由最高管理者(法人代表)或其授權(quán)的代表簽字批準(zhǔn)。
附件4
動(dòng)物試驗(yàn)舉例
一�����、試驗(yàn)?zāi)康?/p>
觀察兔的視網(wǎng)膜光凝反應(yīng)�,熱損傷范圍,并評(píng)估量效關(guān)系��,考核產(chǎn)品治療視網(wǎng)膜疾病的可行性�����、安全性�����。
二��、試驗(yàn)方案設(shè)計(jì)基本要求
1.可選擇設(shè)對(duì)照組��。選擇已在中國(guó)獲準(zhǔn)上市����、具有相同的適用范圍的眼科激光光凝機(jī)進(jìn)行隨機(jī)平行對(duì)照。試驗(yàn)組和對(duì)照組光凝位點(diǎn)應(yīng)在眼底相同的象限內(nèi)的相近點(diǎn)位�。眼內(nèi)各組織生理狀態(tài)、光凝點(diǎn)數(shù)量應(yīng)相當(dāng)�,光凝機(jī)能量參數(shù)設(shè)置應(yīng)相同/相似。象限區(qū)域及光凝點(diǎn)位的設(shè)置應(yīng)確保照射光斑不重疊�,光斑之間的間隔應(yīng)滿足臨床需求。應(yīng)設(shè)置可反映申報(bào)產(chǎn)品量效關(guān)系的能量參數(shù)進(jìn)行試驗(yàn)�����,且應(yīng)當(dāng)能夠涵蓋產(chǎn)品技術(shù)要求中的性能參數(shù)范圍��,如波長(zhǎng)����、光斑大小、激光輸出方式����、功率、脈寬及脈沖間隔(若有)��、占空比(若有)等關(guān)鍵參數(shù)�����。
2.確保每次光凝前,眼組織都處于相同的生理狀態(tài)���,且能證明可用于開展動(dòng)物試驗(yàn)����。通過(guò)OCT反映眼底視網(wǎng)膜各層厚度��,通過(guò)眼底照相機(jī)成眼底彩照反映眼底狀態(tài)�,應(yīng)能滿足開展動(dòng)物試驗(yàn)的要求。
3.評(píng)估試驗(yàn)過(guò)程應(yīng)滿足動(dòng)物試驗(yàn)方法學(xué)的需要���,至少應(yīng)當(dāng)包括:評(píng)估設(shè)備及操作人員應(yīng)相同�����,觀察時(shí)間點(diǎn)應(yīng)統(tǒng)一���,評(píng)估標(biāo)準(zhǔn)應(yīng)統(tǒng)一,并應(yīng)對(duì)評(píng)估者設(shè)盲��。
4.試驗(yàn)之前應(yīng)對(duì)操作人員進(jìn)行充分的培訓(xùn)�,使其充分了解各工作模式(設(shè)置參數(shù))的選擇原則���,在試驗(yàn)時(shí)�����,由操作者針對(duì)每次凝固的組織情況選取適當(dāng)?shù)墓ぷ髂J剑ㄔO(shè)置參數(shù))�����。應(yīng)對(duì)病理評(píng)價(jià)/閱片者設(shè)盲���,病理學(xué)評(píng)價(jià)的人員應(yīng)具有相應(yīng)的資質(zhì)�。試驗(yàn)組和對(duì)照組試驗(yàn)應(yīng)由相同操作者進(jìn)行�,動(dòng)物試驗(yàn)操作人員也應(yīng)當(dāng)持證上崗。
三����、評(píng)價(jià)指標(biāo)
1.主要評(píng)價(jià)指標(biāo)應(yīng)包含:視網(wǎng)膜組織形態(tài)學(xué)及組織病理學(xué)變化。次要評(píng)價(jià)指標(biāo):與激光光凝術(shù)前相比��,是否存在視網(wǎng)膜前和視網(wǎng)膜下的纖維化及增殖��、視網(wǎng)膜出血�����、新生血管形成、激光斑擴(kuò)大����、視網(wǎng)膜水腫等。
2.光凝反應(yīng)�,應(yīng)分析術(shù)前、術(shù)后的視網(wǎng)膜厚度�、脈絡(luò)膜厚度、光斑大小及形態(tài)變化情況����,術(shù)后時(shí)間點(diǎn)可設(shè)置為術(shù)后即刻、24小時(shí)�����、7天�����、1個(gè)月�����?����?蓪?duì)試驗(yàn)動(dòng)物進(jìn)行梯度功率的光凝�。對(duì)照組與試驗(yàn)組能量參數(shù)的選取應(yīng)當(dāng)相同或相似,且滿足臨床需求����。試驗(yàn)結(jié)果應(yīng)給出能量(梯度功率)與術(shù)前術(shù)后視網(wǎng)膜、脈絡(luò)膜厚度變化的量效關(guān)系圖��,應(yīng)至少包含組別�、波長(zhǎng)、工作模式�����、功率范圍��、視網(wǎng)膜�����、脈絡(luò)膜厚度值����;梯度功率可通過(guò)滴定法實(shí)施���,摸索治療視網(wǎng)膜脈絡(luò)膜疾病的有效能量參數(shù)范圍。通過(guò)組織病理學(xué)評(píng)價(jià)分子水平的變化��。
3.熱損傷范圍
(1)應(yīng)給出光凝機(jī)不同波長(zhǎng)�����、不同激光輸出方式下對(duì)試驗(yàn)動(dòng)物的視網(wǎng)膜熱損傷閾值的評(píng)價(jià)�。對(duì)試驗(yàn)動(dòng)物實(shí)施梯度功率光凝后(時(shí)間點(diǎn)設(shè)置同光凝觀察點(diǎn),通過(guò)OCT����、組織病理學(xué)觀察末次點(diǎn)),可通過(guò)檢眼鏡/裂隙燈顯微鏡觀察視網(wǎng)膜損傷斑����,計(jì)算損傷發(fā)生率(損傷斑數(shù)/照射斑數(shù))。按照射梯度功率繪制損傷發(fā)生率與能量的關(guān)系表�����。內(nèi)容應(yīng)包含組別����、波長(zhǎng)�、工作模式�����、功率范圍���、入射總能量范圍、照射斑數(shù)�����、損傷斑數(shù)��。
(2)可以采用組織病理學(xué)或OCT等方法對(duì)熱損傷情況進(jìn)行評(píng)估��。應(yīng)評(píng)估不同時(shí)間點(diǎn)����,試驗(yàn)組與對(duì)照組的凝固帶最大寬度及最大深度、水腫�����、細(xì)胞空泡化等情況���,提供對(duì)比表并附圖����。
4.視網(wǎng)膜的組織病理學(xué)觀察
光凝反應(yīng):用常規(guī)組織病理學(xué)(HE染色)觀察視網(wǎng)膜、脈絡(luò)膜厚度的變化�,觀察激光對(duì)視網(wǎng)膜各層細(xì)胞結(jié)構(gòu)的影響,分析各層細(xì)胞的厚度����,分析視網(wǎng)膜總厚度,以及內(nèi)叢層厚度��、內(nèi)核層厚度�����、外叢層厚度�、外核層厚度、感光細(xì)胞層厚度與視網(wǎng)膜總厚度的比值�。用PAS染色和NG2染色觀察激光對(duì)視網(wǎng)膜微血管形態(tài)的影響,分析視網(wǎng)膜新生血管形成情況與周細(xì)胞缺失后形成的空斑化情況�。可以通過(guò)掃描電鏡觀察光凝反應(yīng)�。
熱損傷范圍:用常規(guī)組織病理學(xué)(HE染色)觀察凝固帶的最大寬度與最大深度,或涉及的細(xì)胞層,觀察視網(wǎng)膜水腫�����、滲漏等情況�。
四、試驗(yàn)報(bào)告
動(dòng)物試驗(yàn)報(bào)告應(yīng)包括但不限于以下內(nèi)容:動(dòng)物模型選擇依據(jù)簡(jiǎn)介�、試驗(yàn)的質(zhì)量保證聲明及相關(guān)證明資料、試驗(yàn)?zāi)康?����、試?yàn)計(jì)劃�、試驗(yàn)材料�����、試驗(yàn)機(jī)及對(duì)照機(jī)(若有)情況�、試驗(yàn)用設(shè)備和機(jī)器及藥品情況、試驗(yàn)結(jié)果及結(jié)論�。
試驗(yàn)機(jī)及對(duì)照機(jī)情況應(yīng)明確:試驗(yàn)機(jī)的主機(jī)及附件,對(duì)照機(jī)的醫(yī)療器械注冊(cè)證書編號(hào)及試驗(yàn)機(jī)的主機(jī)及附件���。
試驗(yàn)計(jì)劃中應(yīng)詳述樣本量及分組�����,應(yīng)說(shuō)明動(dòng)物的數(shù)量和分組�����。明確每只動(dòng)物光凝的眼部象限區(qū)域和各區(qū)域的光凝點(diǎn)數(shù)量�����。應(yīng)對(duì)試驗(yàn)環(huán)境��、試驗(yàn)步驟進(jìn)行描述�����,明確樣品準(zhǔn)備�����、動(dòng)物準(zhǔn)備��、手術(shù)方法�����、手術(shù)部位、術(shù)前準(zhǔn)備等�。應(yīng)對(duì)手術(shù)過(guò)程進(jìn)行詳細(xì)描述。應(yīng)給出評(píng)價(jià)指標(biāo)及評(píng)價(jià)標(biāo)準(zhǔn)���。
試驗(yàn)結(jié)果及結(jié)論應(yīng)對(duì)眼科激光光凝機(jī)包括輸出端的試驗(yàn)結(jié)果進(jìn)行整體評(píng)價(jià)���。應(yīng)提供完整的數(shù)據(jù)報(bào)告,包括:每種波長(zhǎng)在每種激光輸出方式的應(yīng)用情況����,主要評(píng)價(jià)指標(biāo)和次要評(píng)價(jià)指標(biāo)。數(shù)量設(shè)備編號(hào)����,樣本編號(hào),各評(píng)價(jià)指標(biāo)的試驗(yàn)結(jié)果及其分析等�。熱損傷報(bào)告應(yīng)提供高質(zhì)量的彩色圖像����,并應(yīng)清楚標(biāo)明損傷區(qū)域邊緣及測(cè)量方法。